[考点]
氧气的化学性质,酸的化学性质,碱的化学性质,中和反应及其应用,酸雨的产生、危害及防治,铵态氮肥的检验,
[答案]
(1)溶液由红色变成无色;固体溶解,溶液由无色变黄色;ABD。
(2)不正确。
(3)①二氧化碳能够溶于水,也能使试管中的液面上升。
②能。
(4)减少含硫物质的燃烧。
[解析]
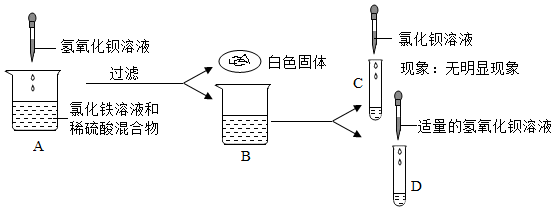
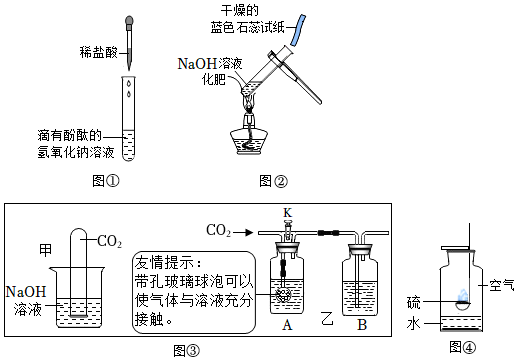
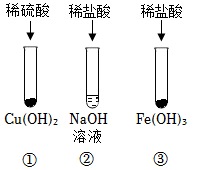
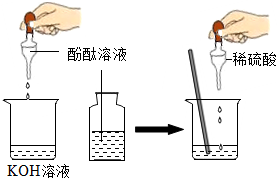
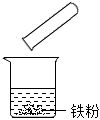
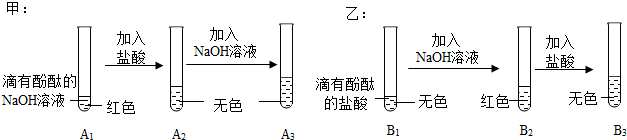
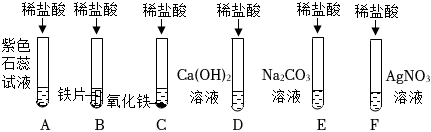
解:(1)图①中证明氢氧化钠溶液和稀盐酸能发生反应的现象是溶液由红色变成无色(氢氧化钠溶液显碱性,能使酚酞变红色,和稀盐酸完全反应后溶液显酸性或显中性,),实验结束后,为了验证稀盐酸是否加过量,小梁同学取样于试管中,加入适量的氧化铁,从而证明了稀盐酸确实加过量,小梁的实验中观察到固体溶解,溶液由无色变黄色(盐酸和氧化铁反应生成氯化铁和水),小梁同学又选择了以下药品证明盐酸过量,其中可行的是铁(铁和盐酸反应生成氯化亚铁和氢气,观察到固体溶解、溶液由无色变成浅绿色)、碳酸钠溶液(碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,过程中产生气泡)、氢氧化镁(稀盐酸和氢氧化镁反应生成氯化镁和水,过程中固体溶解)。
故答案为:溶液由红色变成无色;固体溶解,溶液由无色变黄色;ABD。
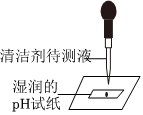
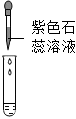
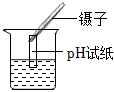
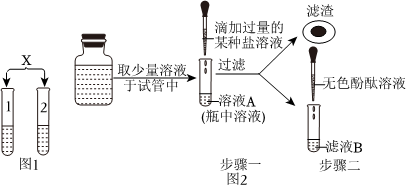
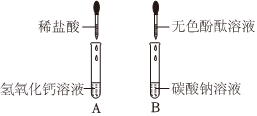
(2)为了检验某化肥是否为铵态氮肥,图②实验所用试纸不正确,应该用湿润的红色石蕊试纸,是因为氨气不能使石蕊变色,氨气和水反应生成氨水,氨水显碱性,能使湿润红色石蕊试纸变蓝色。
故答案为:不正确。
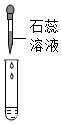
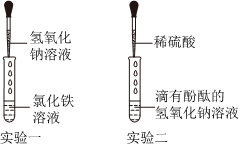
(3)①实验甲中,小欣观察到试管内液面上升,该现象无法说明二氧化碳和氢氧化钠能发生反应,原因是二氧化碳能够溶于水,也能使试管中的液面上升。
故答案为:二氧化碳能够溶于水,也能使试管中的液面上升。
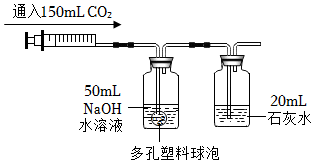
②向A中加入100mL的NaOH溶液,向B中加入100mL的Ca(OH)2溶液,关闭K,通入约600mL二氧化碳,发现A和B中均无明显现象,该实验能说明二氧化碳和氢氧化钠发生了反应,是因为如果不能反应,则600mL二氧化碳不能完全溶解在100mL的NaOH溶液中,导致部分二氧化碳进入澄清石灰水中,能使澄清石灰水变浑浊。
故答案为:能。
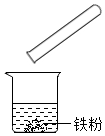
(4)图④实验为硫在空气中燃烧的实验,二氧化硫是形成酸雨的主要物质,减少酸雨的措施是减少含硫物质的燃烧等。
故答案为:减少含硫物质的燃烧。
[点评]
本题考查了"氧气的化学性质,酸的化学性质,碱的化学性质,中和反应及其应用,酸雨的产生、危害及防治,铵态氮肥的检验,",属于"压轴题",熟悉题型是解题的关键。
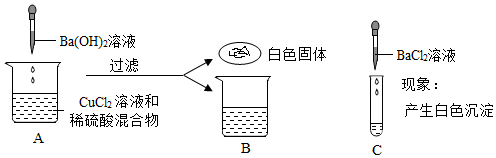
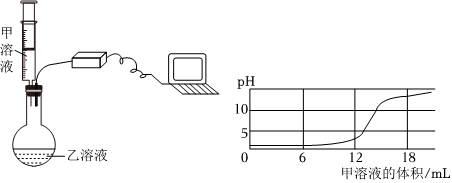
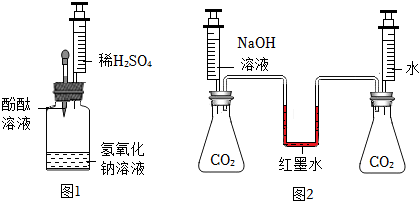

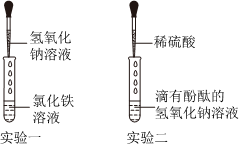
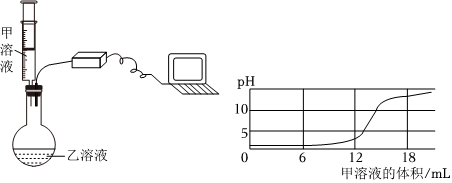
 学习小组同学进行了如图所示的实验,并展开了拓展学习与探究。
学习小组同学进行了如图所示的实验,并展开了拓展学习与探究。