[考点]
实验探究物质的组成成分以及含量,酸的化学性质,碱的化学性质,
[答案]
【讨论分析】氢氧化钠不能与碳酸钙、氢氧化镁反应;
【实验探究】一;
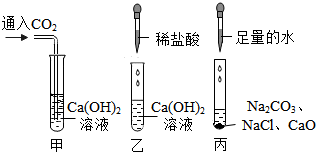
【设计实验】(1)澄清石灰水变浑浊;
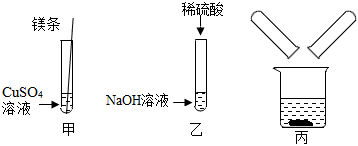
(2)2NaOH+MgCl2=Mg(OH)2↓+2NaCl;
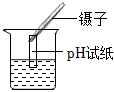
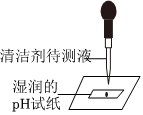
【反思与交流】(1)错误之处是pH试纸被湿润,导致测定的显酸性溶液结果偏高。
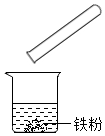
(2)酸具有腐蚀性,且酸能与活泼金属反应。
[解析]
解:【讨论分析】由于氢氧化钠与碳酸钙、氢氧化镁均不能反应,即不能除去水垢,则猜想三不成立。
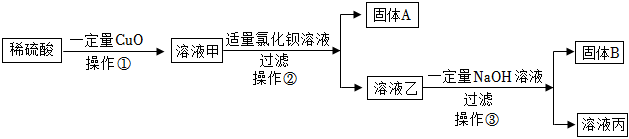
【实验探究】步骤Ⅱ:由于硫酸能与氯化钡反应生成硫酸钡沉淀和盐酸,但盐酸不能与氯化钡反应,现象为无明显现象,则说明溶液中不含硫酸,则猜想一成立。
【设计实验】(1)由于盐酸能与碳酸钙反应生成二氧化碳气体,二氧化碳能使澄清石灰水变浑浊,则现象为澄清石灰水变浑浊。
(2)盐酸能与氢氧化镁反应生成氯化镁和水,氯化镁能与氢氧化钠反应生成氢氧化镁沉淀和氯化钠,则反应的化学方程式为2NaOH+MgCl2=Mg(OH)2↓+2NaCl。
【反思与交流】(1)上述实验操作步骤中错误之处及其会造成的后果是错误之处是pH试纸被湿润,导致测定的显酸性溶液结果偏高。
(2)由于酸具有腐蚀性,且酸能与活泼金属反应,则使用该清洁剂时要戴手套且勿与金属物品接触。
故答案为:【讨论分析】氢氧化钠不能与碳酸钙、氢氧化镁反应;
【实验探究】一;
【设计实验】(1)澄清石灰水变浑浊;
(2)2NaOH+MgCl2=Mg(OH)2↓+2NaCl;
【反思与交流】(1)错误之处是pH试纸被湿润,导致测定的显酸性溶液结果偏高。
(2)酸具有腐蚀性,且酸能与活泼金属反应。
[点评]
本题考查了"实验探究物质的组成成分以及含量,酸的化学性质,碱的化学性质,",属于"难典题",熟悉题型是解题的关键。
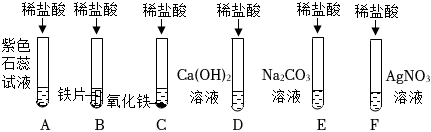
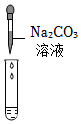
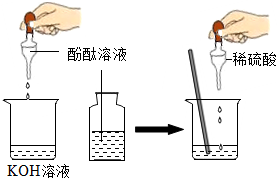
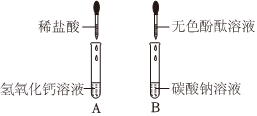 学习小组同学进行了如图所示的实验,并展开了拓展学习与探究。
学习小组同学进行了如图所示的实验,并展开了拓展学习与探究。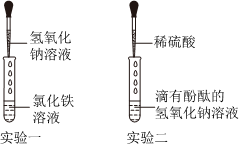
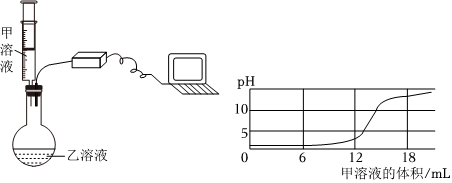
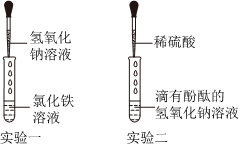
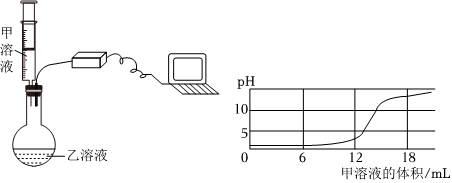
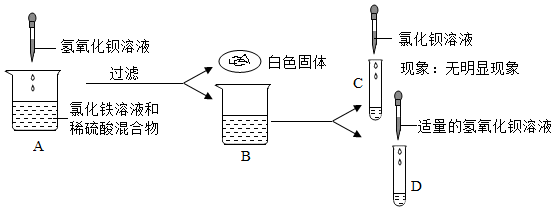
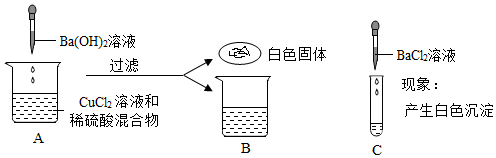
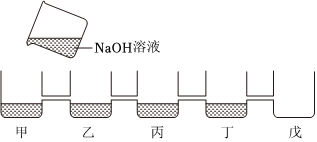
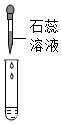
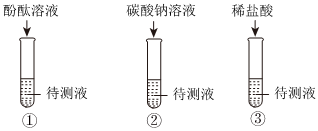 学习小组的同学和老师一起整理实验台时,发现有一瓶失去标签的无色溶液,据老师回忆,可能是NaOH溶液或Ca(OH)2溶液,为了鉴别该无色溶液,同学们进行如下实验:
学习小组的同学和老师一起整理实验台时,发现有一瓶失去标签的无色溶液,据老师回忆,可能是NaOH溶液或Ca(OH)2溶液,为了鉴别该无色溶液,同学们进行如下实验: