[考点]
实验探究物质的性质或变化规律,盐的化学性质,
[答案]
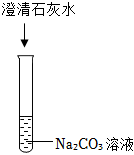
(1)有白色沉淀产生;
(2)无;
(3)HCl+NaOH=NaCl+H2O;
(4)新物质;
(5)C;
(6)三或3。
[解析]
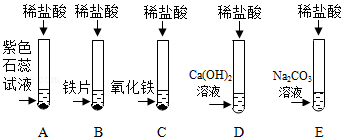
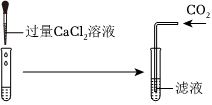
解:(1)硝酸银和盐酸反应生成氯化银沉淀和硝酸,则可观察到有白色沉淀产生。故答案为:有白色沉淀产生;
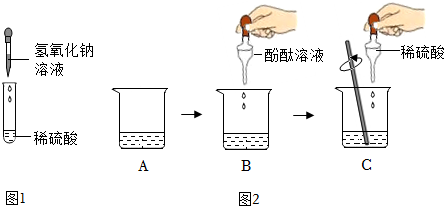
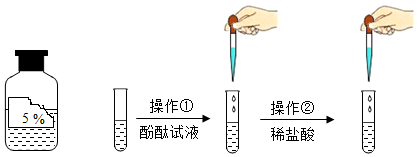
(2)氢氧化钠溶液显碱性,能使酚酞溶液变红色,则滴加酚酞溶液后,若酚酞呈无色,说明溶液中不含氢氧化钠,则可证明盐酸和氢氧化钠发生了化学反应。故答案为:无;
(3)氢氧化钠和盐酸反应生成氯化钠和水,反应的化学方程式为:HCl+NaOH=NaCl+H2O。故答案为:HCl+NaOH=NaCl+H2O;
(4)结合前面实验探究,可知对于无明显现象的反应,证明反应发生的思路为:验证生成的新物质或验证反应物的消失。故答案为:新物质;
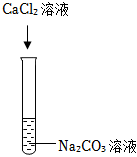
(5)A、氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,会引入新杂质氯化钠,故错误;
B、碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,且盐酸和氢氧化钠反应生成氯化钠和水,既除去了杂质,也除去了主要物质,故错误;
C、碳酸钠和氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,既能除去杂质,也不引入新杂质,该正确。
故选:C。
(6)甲中氢氧化钠和盐酸反应生成氯化钠和水,乙中氯化钠和氯化氢不反应,C中碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,D中硝酸银和盐酸反应生成氯化银和硝酸,由于溶液pH>7,溶液显碱性,则溶液中一定不存在硝酸银、盐酸和硝酸,一定含有氯化钠和硝酸钠(显碱性的氢氧化钠或碳酸钠都和硝酸反应会产生硝酸钠),可能含有氢氧化钠或碳酸钠中的一种或两种,则共有三种可能。故答案为:三或3。
[点评]
本题考查了"实验探究物质的性质或变化规律,盐的化学性质,",属于"必考题",熟悉题型是解题的关键。
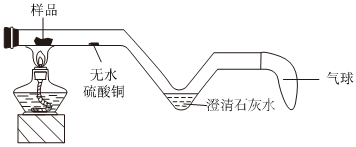
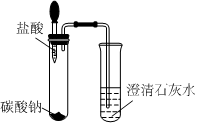
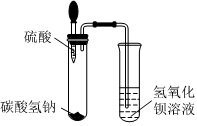
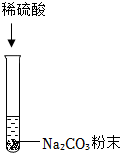
 兴趣小组同学自制呼吸面具,准备用过氧化钠(Na2O2)作为供氧剂,但在实验室找到了一瓶敞口放置的过氧化钠。
兴趣小组同学自制呼吸面具,准备用过氧化钠(Na2O2)作为供氧剂,但在实验室找到了一瓶敞口放置的过氧化钠。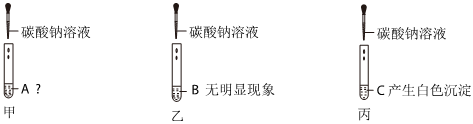
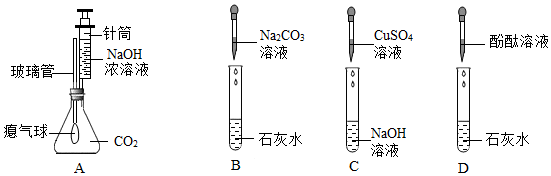
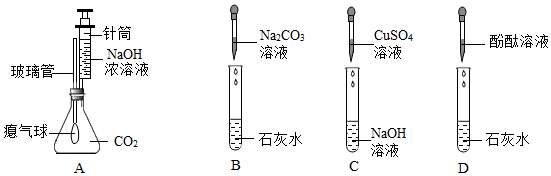
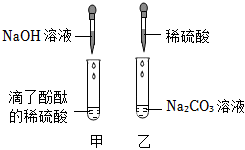
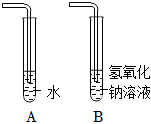
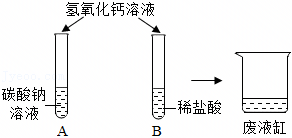
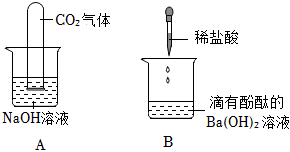 实验课上,某化学小组探究两个初中常见的无明显现象的反应:甲同学利用装置A将装满CO2的试管倒扣在盛有NaOH溶液的烧杯中,乙同学借助无色酚酞溶液利用装置B进行中和反应,如图所示:
实验课上,某化学小组探究两个初中常见的无明显现象的反应:甲同学利用装置A将装满CO2的试管倒扣在盛有NaOH溶液的烧杯中,乙同学借助无色酚酞溶液利用装置B进行中和反应,如图所示: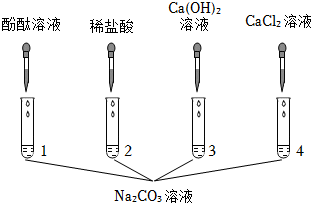 ?
?