服务热线
搜题▪组卷
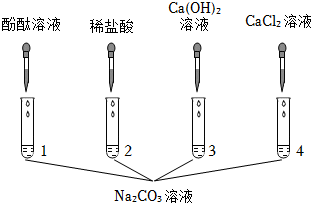
| 实验步骤 | 实验现象 | 结论 |
| 取少量实验1所得溶液于试管中滴加足量氯化钙溶液 | 白色沉淀 | 猜想一成立 |
| 【观察与问题】 | 【实验与事实】 | 【解释与结论】 | ||
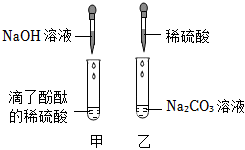
| 分别向AB两支试管中通入CO2 | 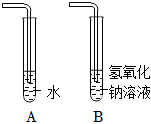 |
甲同学再向A试管中滴入紫色石蕊溶液,溶液变红 | 有酸性物质生成 | 证明有新物质生成 |
| 乙同学再向B试管中滴入少量氯化钡溶液,有 。 | 氢氧化钠和二氧化碳反应生成了碳酸钠 | |||
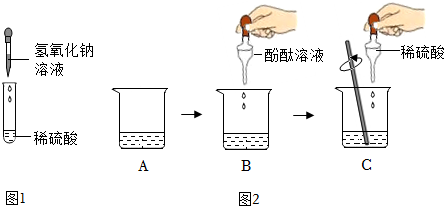
| 方法 | 实验操作 | 实验现象 | 实验结论 | |
| (1) | 取少量溶液C,滴入几滴 溶液 | 有红褐色沉淀生成 | 溶液中有NaOH | 发生了化学反应 |
| (2) | 取少量溶液C于试管中,插入打磨过的铁丝 | 溶液中没有硫酸 | ||
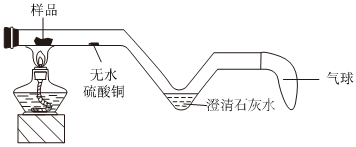
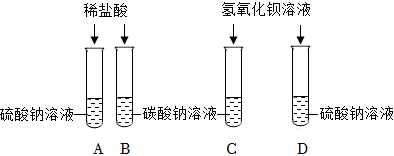
| 组别 | 甲组 | 乙组 |
| 实验操作 |
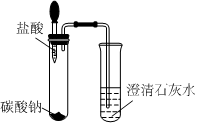 |
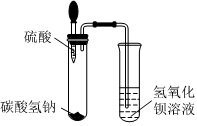 |
| 实验现象 | 试管中有气泡产生,澄清石灰水未变浑浊 | 试管中有气泡产生,有白色沉淀生成 |
| 实验结论 | 碳酸钠能与盐酸反应,但不产生CO2 | 碳酸氢钠能与硫酸反应,产生CO2 |
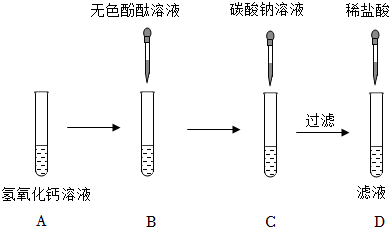
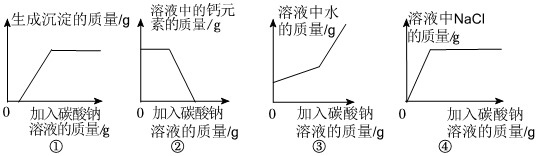
| 实验操作设想 | 预测实验现象 | 预测实验结论 |
| ①取少量废液于试管中,滴加足量的BaCl2溶液。 | 产生白色沉淀,溶液为红色 | 猜想 不成立 |
| ②继续向①的试管中滴加足量的稀硝酸。 | 白色沉淀不溶解,溶液为无色 | 猜想三成立 |
| ,溶液为无色 | 猜想四成立 |
 ?
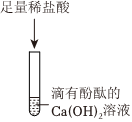
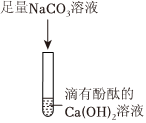
?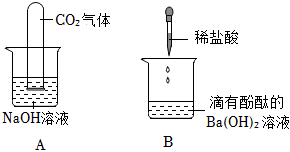 实验课上,某化学小组探究两个初中常见的无明显现象的反应:甲同学利用装置A将装满CO2的试管倒扣在盛有NaOH溶液的烧杯中,乙同学借助无色酚酞溶液利用装置B进行中和反应,如图所示:
实验课上,某化学小组探究两个初中常见的无明显现象的反应:甲同学利用装置A将装满CO2的试管倒扣在盛有NaOH溶液的烧杯中,乙同学借助无色酚酞溶液利用装置B进行中和反应,如图所示: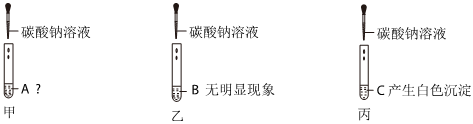
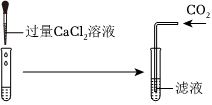
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入过量稀盐酸 | 无明显现象 | 猜想 正确 |
| 另取少量滤液于试管中,加入过量Na2CO3溶液 |
 兴趣小组同学自制呼吸面具,准备用过氧化钠(Na2O2)作为供氧剂,但在实验室找到了一瓶敞口放置的过氧化钠。
兴趣小组同学自制呼吸面具,准备用过氧化钠(Na2O2)作为供氧剂,但在实验室找到了一瓶敞口放置的过氧化钠。| 实验编号 | 实验操作 | 实验现象 | 实验结论 |
| 甲 | 向试管1中滴加足量稀盐酸 | 有气泡产生 | 猜想 不正确 |
| 乙 | 向试管2中滴加Ca(OH)2溶液至不再有白色沉淀生成,向上层清液中滴加几滴无色酚酞试液 | 溶液变红 | 猜想三正确 |
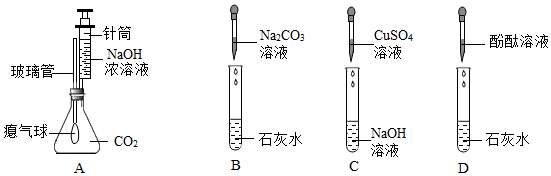
| 实验操作 | 实验现象 | 结论 |
| 在试管甲中滴加碳酸钠溶液 | 未产生白色沉淀 | 猜想 错误 |
| 在试管乙中滴加足量的稀盐酸 | 猜想二正确 |
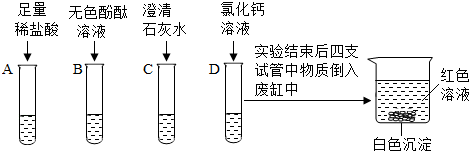
| 实验方案 | 实验现象 | 实验结论 | |
| 小田同学 | 取少量废液缸中上层红色溶液于试管中,加入过量的BaCl2溶液 | 观察到 | 猜想二成立 |
| 小威同学 | 取少量废液缸中上层红色溶液于试管中,加入过量的Ba(OH)2溶液 |
| 实验步骤 | 现象 | 实验结论 | |
| 取过滤后的溶液各少许,分别装在2支试管里 | ①向第一支试管中滴加少量稀盐酸 | 无明显现象 | 猜想Ⅱ错误 |
| ②向第二支试管液中加入Na2CO3 | 猜想Ⅲ正确 | ||
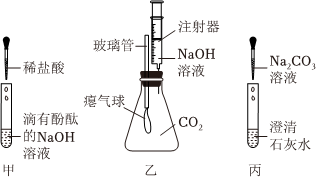
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量丙中上层清液于试管中,滴加BaCl2溶液 | 猜想二不成立 | |
| ②另取少量丙中上层清液于试管中,滴加K2CO3溶液 | 有白色沉淀产生 | 猜想 成立 |
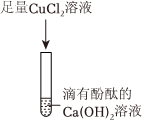
| 实验操作 | 实验现象 | 实验结论 | |
| 取少量烧杯内的上层清液于试管中 | ①向试管中加入过量BaCl2溶液 | 产生白色沉淀 | 清液中一定还含有Na2CO3和NaOH。 |
| ②将①所得物质过滤,得到滤渣和滤液,取滤液于试管中,加入无色酚酞溶液 | 溶液变红色 | ||
| ③取滤渣于试管中,加入过量稀硝酸 | |||
| 实验操作 | 实验现象 | 实验结论 |
| 步骤1:取少量废液于试管中,加入过量的氯化钙溶液 | ① 。 | 废液中有K2CO3 |
| 步骤2:取少量步骤1所得的上层清液,向其中加入硫酸铜溶液 | 有蓝色絮状沉淀产生 | ②废液中有 。 |

jr@dyw.com
2025-03-07
初中化学 | | 实验探究题