服务热线
搜题▪组卷
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量污水于一支洁净试管中,向其中滴加少量的Ba(NO3)2溶液 | 污水中一定不含有硫酸 | |
| ②另取少量污水于一支洁净试管中,向其中滴加少量的 (填化学式)溶液 | 有白色沉淀生成 | 污水中一定含有盐酸 |
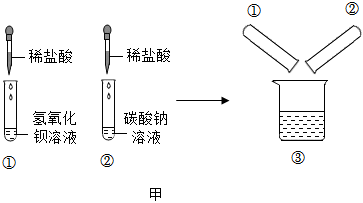
| 组别 | 废液缸中现象 | 现象解释 |
| 第1小组 | 无沉淀、有气泡产生 | |
| 第2小组 | 无沉淀、无气泡产生 | |
| 第3小组 | … | |
| … | … |
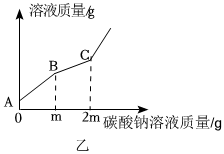
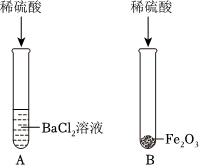
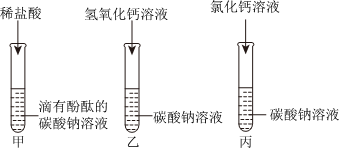
| 方案 | 实验操作 | 实验现象 | 结论 |
| 一 | 取少量烧杯中的溶液于试管中,加入过量 溶液 | 先有气泡产生,后有白色沉淀生成 | 猜想二正确 |
| 二 | 取少量烧杯中的溶液于试管中,加入锌粒 |
| 滤液1 | 滤液2 | 滤液3 | 滤液4 | |
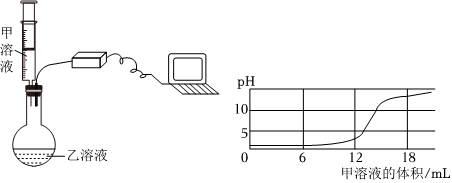
| 测得的pH | 5 | 6 | 6 | 5 |
| 实验步骤 | 实验现象 | 实验结论 | |
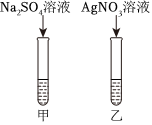
| ① | 取滤液于试管中,加入足量稀硝酸,无明显现象。而后滴加过量Ba(NO3)2溶液 | 产生白色沉淀 | 含有硫酸根离子 |
| ② | 静置并取步骤①中上层清液于试管中,滴加 溶液 | 产生白色沉淀 | 含有氯离子 |
| ③ | 另取适量土壤样品,加熟石灰混合研磨 | 有刺激性气味的气体产生 | 含有 离子 |
| 所用物质 | |
| 改良酸性土壤 | 熟石灰[Ca(OH)2] |
| 草木灰(主要成分为K2CO3) | |
| 改良碱性土壤 | 硫酸亚铁(FeSO4) |
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量反应后的溶液于试管中,滴加酚酞试液 | __________ | 猜想一不正确 |
| ②另取少量反应后的溶液于试管中,加入 ____溶液 | 无气泡产生 | 猜想二不正确 |
| 实验操作 | 实验现象 | 实验结论 |
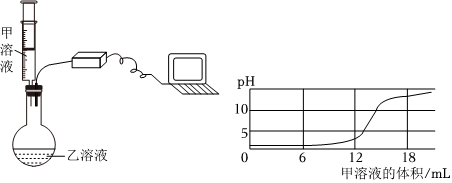
步骤Ⅰ:取少量样品,进行如图操作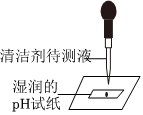 |
pH=5 | 该溶液呈酸性 |
| 步骤Ⅱ:取少量样品,加入蒸馏水稀释后,滴入氯化钡溶液 | 无明显现象 | 猜想 成立 |
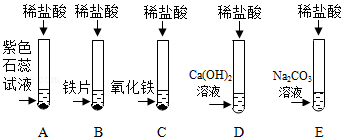
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,滴加适量的碳酸钠溶液 | 猜想二不成立 | |
| 取少量滤液于试管中,滴加 | 产生白色沉淀 | 猜想四成立 |
| 实验 | 操作 | 现象 |
| ① | 向沉淀中加入足量稀硝酸 | 沉淀部分消失,有气泡产生 |
| ② | 向溶液中加入过量稀硫酸 | 只有白色沉淀产生 |
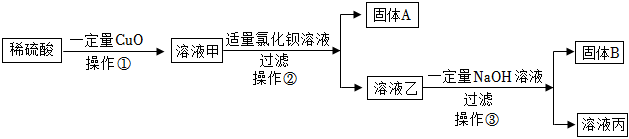
| 实验方案 | 实验现象 | 实验结论 |
| 方案一:取适量溶液丙于试管内,向其中滴加硫酸铵溶液,管口放置湿润的红色石蕊试纸,微热。 | 试纸变 色。 | 猜想二成立。 |
| 方案二:用玻璃棒蘸取适量溶液丙,滴于湿润的pH试纸上,待显色后与标准比色卡对照读数。 | pH=12。 |
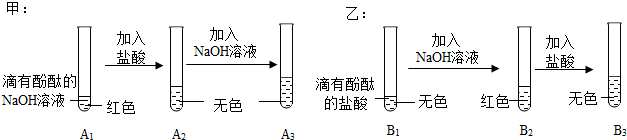
| 探究环节 | 甲同学的探究 | 乙同学的探究 |
| 提出问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
| 做出猜想 | 实验过程中,酚酞变质了? | 猜想一:NaCl 猜想二:NaCl HCl |
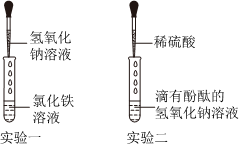
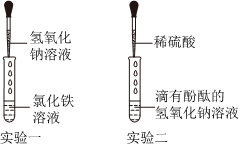
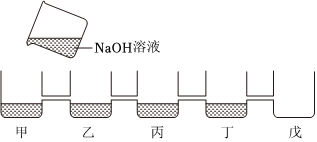
| 实验验证 | (1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想 (填“成立”或“不成立”) (2)你认为,在常温下A2溶液测出的pH 应 (填“>”、“=”或“<”)7 |
取少量B3溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变 ,据此,你认为乙同学的猜想 (填“一”或“二”)成立 |
| 交流反思 | (1)甲、乙同学的实验中,反应均涉及到的化学方程式是 。 (2)A3溶液未变红,你认为原因是A2溶液中 盐酸 较多,加入的NaOH溶液未将其完全中和。 (3)甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制。 |
|

fik@dyw.com
2023-04-15
初中化学 | 九年级下 | 实验探究题