[考点]
实验探究物质的组成成分以及含量,酸的化学性质,碱的化学性质,盐的化学性质,
[答案]
(1)红;
(2)2NaOH+H2SO4=Na2SO4+2H2O;
(3)MgSO4;
(4)Ⅱ;硫酸与氢氧化镁沉淀不能共存;
(5)溶液变为蓝色。
[解析]
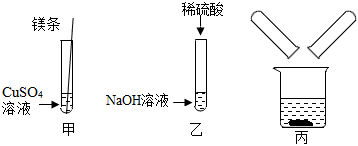
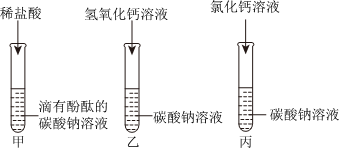
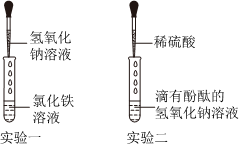
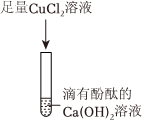
解:(1)由于金属活动性Mg>Cu,实验甲中,镁与硫酸铜反应生成铜和硫酸镁,铜是红色固体,所以可观察到镁条表面附着一层红色固体。
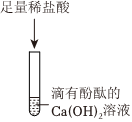
(2)实验乙中,氢氧化钠与硫酸反应生成硫酸钠和水,反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O。
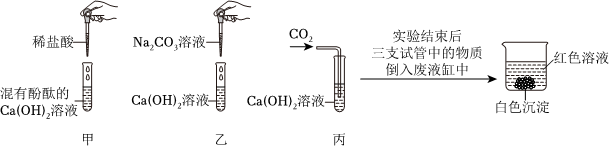
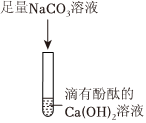
(3)小组同学将两支试管中的废液同时倒入一个洁净的烧杯中,产生白色沉淀,上层为无色澄清溶液知,烧杯内溶液中一定没有硫酸铜和硫酸,产生的白色沉淀是硫酸镁与氢氧化钠反应生成的氢氧化镁,同时还生成了溶于水的硫酸钠,则烧杯内溶液中溶质的成分可能为:Na2SO4或Na2SO4和NaOH或Na2SO4和MgSO4,故猜想Ⅳ为Na2SO4和MgSO4。
(4)经讨论,大家一致认为猜想2是错误的,硫酸与氢氧化镁沉淀不能共存,所以烧杯中一定没有硫酸。
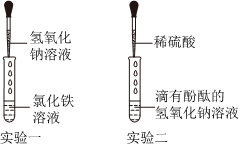
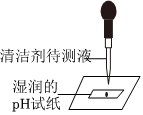
(5)由于实验结论是猜想1成立,即烧杯内溶液中溶质是Na2SO4和NaOH,NaOH能使紫色石蕊溶液变成蓝色,所以取少量烧杯中的溶液于洁净的试管中,加入石蕊试液,出现的实验现象是紫色石蕊溶液变为蓝色。
故答案为:(1)红;
(2)2NaOH+H2SO4=Na2SO4+2H2O;
(3)MgSO4;
(4)Ⅱ;硫酸与氢氧化镁沉淀不能共存;
(5)溶液变为蓝色。
[点评]
本题考查了"实验探究物质的组成成分以及含量,酸的化学性质,碱的化学性质,盐的化学性质,",属于"综合题",熟悉题型是解题的关键。