[考点]
金属活动性的探究,常见金属的冶炼方法,反应类型的判定,
[答案]
(1)增大反应物的接触面积,使反应更快、更充分;
(2)置换反应;
(3)防止锌与氧气在温度较高时反应生成氧化锌;
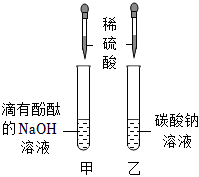
【进行实验】实验1:Mn+2HCl=MnCl2+H2↑;
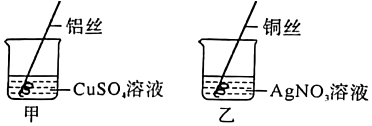
实验2:锰片表面有红色固体生成,溶液由蓝色变为浅粉色;
【讨论交流】A。
[解析]
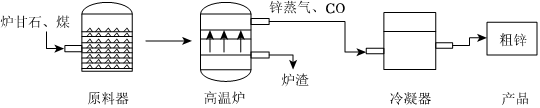
解:(1)装入原料器之前,将炉甘石敲碎的目的是增大反应物的接触面积,使反应更快、更充分;
(2)煤的主要成分是碳,高温炉内,碳酸锌在高温条件下与碳发生反应生成锌和CO,该反应符合一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应;
(3)必须“冷定”后才能“毁罐”取锌,请从化学变化的角度解释其原因是防止锌与氧气在温度较高时反应生成氧化锌;
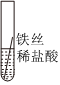
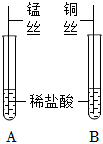
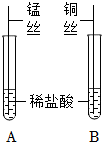
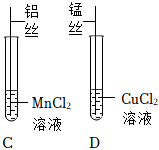
【进行实验】实验1:A试管中锰丝表面有气泡产生,溶液由无色变为浅粉色,说明锰和稀盐酸发生了反应,锰和稀盐酸反应生成氯化锰和氢气,反应的化学方程式为Mn+2HCl=MnCl2+H2↑;
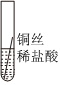
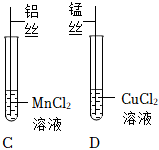
实验2:结论为猜想3成立,则锰比铜活泼,D试管中锰和氯化铜反应生成氯化锰和铜,现象是锰片表面有红色固体生成,溶液由蓝色变为浅粉色;
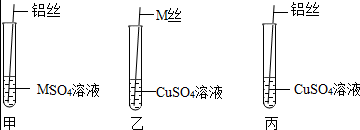
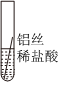
【讨论交流】A、依次插入Mn、Cu、Al,锰和稀硫酸反应生成硫酸锰和氢气,铜和硫酸锰不反应,说明锰的活动性大于铜,铝和硫酸锰反应生成硫酸铝和锰,说明铝的活动性大于锰,可以验证三种金属的活动性顺序,故A符合题意;
B、依次插入Al、Mn、Cu,铝和稀硫酸反应生成硫酸铝和氢气,锰和硫酸铝不反应,说明铝的活动性大于锰,铜和硫酸铝不反应,说明铝的活动性大于铜,无法探究锰、铜的金属活动性顺序,故B不符合题意;
C、依次插入Cu、Mn、Al,铜和稀硫酸不反应,说明铜排在氢后,铝和稀硫酸反应生成硫酸铝和氢气,说明铝在氢前,则铝比铜活泼,锰与硫酸铝不反应,说明铝比铜活泼,无法探究锰、铜的金属活动性顺序,故C不符合题意;
故选:A。
故答案为:(1)增大反应物的接触面积,使反应更快、更充分;
(2)置换反应;
(3)防止锌与氧气在温度较高时反应生成氧化锌;
【进行实验】实验1:Mn+2HCl=MnCl2+H2↑;
实验2:锰片表面有红色固体生成,溶液由蓝色变为浅粉色;
【讨论交流】A。
[点评]
本题考查了"金属活动性的探究,常见金属的冶炼方法,反应类型的判定,",属于"难典题",熟悉题型是解题的关键。
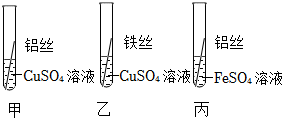
 某化学兴趣小组的同学为了比较金属R与铁、铜的金属活动性强弱,进行如下探究活动。
某化学兴趣小组的同学为了比较金属R与铁、铜的金属活动性强弱,进行如下探究活动。