服务热线
搜题▪组卷
试卷总分:50分 命题人:dyhx2020 考试时长:120分钟
A.经常食用豆奶,可为人体补充丰富的维生素
B.NaHCO3受热分解放出CO2,可用作灭火剂的原料
C.将锅炉燃料煤改气,可减轻大气污染
D.回收利用废旧金属,可节约金属资源
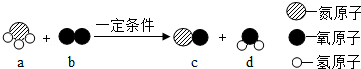
| A.该反应属于置换反应 |
B.氧原子的结构示意图为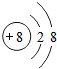
|
| C.b,d两种物质均由分子构成 | D.a物质中氮元素的化合价为+3价 |
| A.茶氨酸由碳、氢、氧、氮四种元素组成 | B.茶氨酸属于有机物,锌、硒指单质 |
| C.一个茶氨酸分子中含有3个氧原子 | D.茶树不宜在碱性土壤中生长 |
A.铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀
B.水和过氧化氢的组成元素相同,则两者的化学性质相同
C.Na+、Mg2+、Cl﹣的最外层电子数均为8,由此得出离子的最外层电子数均为8
D.同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率
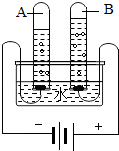

| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | |
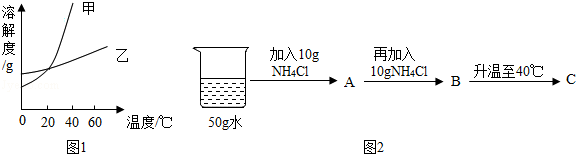
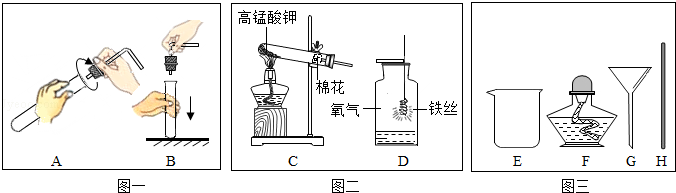
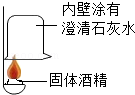
| 方案 | 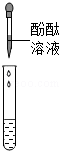 |
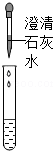 |
| 现象 | 溶液变红 | 产生 白色沉淀 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |

dyhx2020
2014-08-08
初中化学 | 中考 | 难度:3
| 下载试卷 | 收藏 |
| 平行组卷 | 细目重组 |
| 试卷分析 | 加入白板 |
| 加卷篮 | 更多功能 |
平行组卷卷生成中,请等待