[考点]
实验探究物质的组成成分以及含量,酸的化学性质,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式,
[答案]
【猜想假设】③
【实验探究】
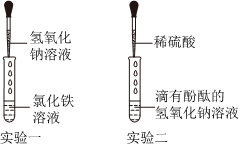
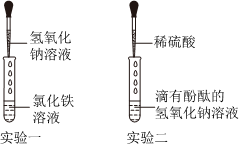
(1)不合理;酚酞试液遇中性和酸性溶液均不变色(合理即可);
(2)CuO+H2SO4═CuSO4+H2O
【实验结论】④
【拓展应用】以免腐蚀下水道钢管(或染污环境)
[解析]
解:
【猜想假设】
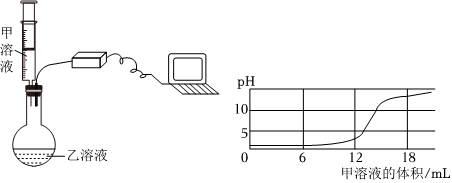
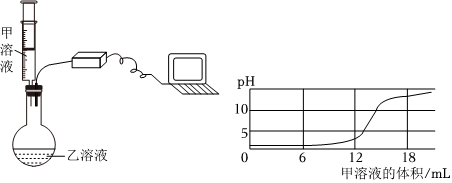
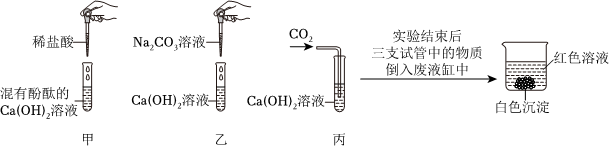
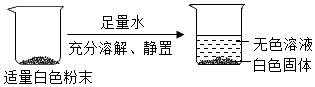
稀硫酸、氢氧化钠溶液和碳酸钠溶液混合一起反应时,如果稀硫酸滴加过快,稀硫酸和碳酸钠反应,开始也会产生气泡,有二氧化碳生成,有可能没把氢氧化钠消耗完,稀硫酸已经没有了,故②合理;碳酸钠和硫酸能反应,不能共存,故③不合理;
【实验探究】
(1)取少量该溶液于试管中,向其中滴加无色酚酞,发现溶液颜色无变化,说明溶液中无碳酸钠和氢氧化钠,故④⑤都符合,因此小鹏的结论是不合理,理由是④Na2SO4、H2SO4也不能使无色酚酞变色;
(2)向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝.说明溶液中有硫酸,反应的化学方程式为:CuO+H2SO4═CuSO4+H2O;
【实验结论】碳酸钠的溶液显碱性,稀硫酸的溶液显酸性,滴加无色酚酞,发现溶液颜色无变化,排除①②,向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝,排除⑤;故④是正确的;
【拓展应用】实验室的酸性废水必须处理至中性再排放可以减少水的污染.
答案:
【猜想假设】③
【实验探究】
(1)不合理;酚酞试液遇中性和酸性溶液均不变色(合理即可);
(2)CuO+H2SO4═CuSO4+H2O
【实验结论】④
【拓展应用】以免腐蚀下水道钢管(或染污环境)
[点评]
本题考查了"实验探究物质的组成成 酸的化学性质 碱的化学性质 盐的化学性质 书写化学方程式、文字 ",属于"综合题",熟悉题型是解题的关键