[考点]
实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,
[答案]
【做出猜想】
氢、碳、氧。
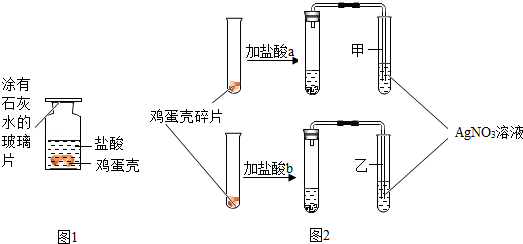
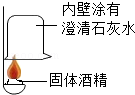
【实验1】
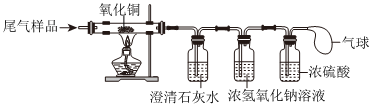
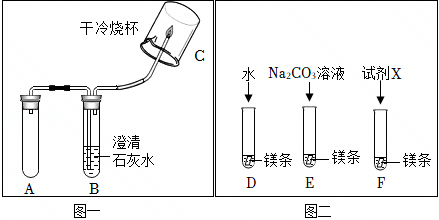
气体通过B装置带出水蒸气。
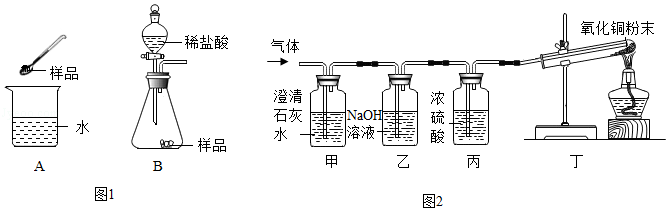
【实验2】
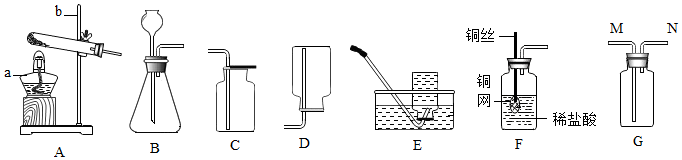
(1)对比。
(2)氢氧化钠溶液。
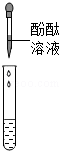
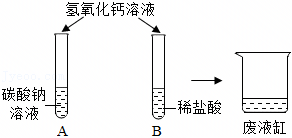
【实验3】
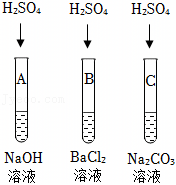
MgCO3+2HCl=MgCl2+H2O+CO2↑。
[解析]
解:【做出猜想】
小组同学经查阅资料和讨论,根据化学变化过程中元素不变,且反应物中含有氢、碳、氧元素,做出如下猜想:①产生的气体为氢气;②产生的气体为二氧化碳;②产生的气体为氢气和二氧化碳。
故答案为:氢、碳、氧。
【实验1】
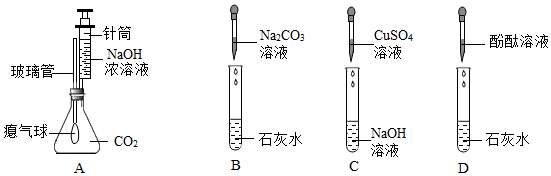
小组同学讨论后认为:C中烧杯内壁有水珠产生不能作为A中有氢气产生的的依据。其原因是气体通过B装置带出水蒸气。
故答案为:气体通过B装置带出水蒸气。
【实验2】
(1)D实验的作用是对比。
故答案为:对比。
(2)试剂X是氢氧化钠溶液(氢氧化钠溶液中含有氢氧根离子和钠离子,能够验证钠离子和氢氧根离子能否促进反应进行)。
故答案为:氢氧化钠溶液。
【实验3】
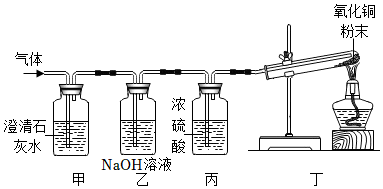
取实验1反应生成的沉淀于试管中,加入足量稀盐酸,根据实验现象可说明白色沉淀中有MgCO3,碳酸镁和稀盐酸反应生成氯化镁、水和二氧化碳,发生反应的化学方程式为MgCO3+2HCl=MgCl2+H2O+CO2↑。
故答案为:MgCO3+2HCl=MgCl2+H2O+CO2↑。
[点评]
本题考查了"实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,",属于"易错题",熟悉题型是解题的关键。
 ?
?