服务热线
搜题▪组卷
| 实验编号 试剂 |
甲 | 乙 | 丙 | 丁 |
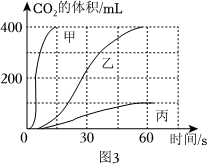
| mg大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
| ng盐酸(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
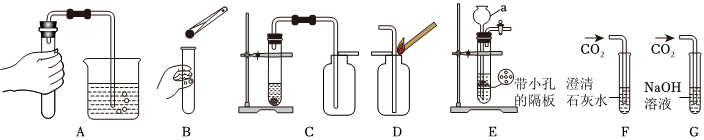
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 甲同学 | 取少量样品溶液于试管中,滴加 溶液 | 有气泡产生 | 猜想一不成立 |
| 乙同学 | ①先另取少量样品溶液于试管中,加入过量氯化钡溶液 | 猜想 成立 | |
| ②然后静置,向反应后的上层清液中,滴加2~3滴的无色酚酞溶液 | 上层清液变红 |
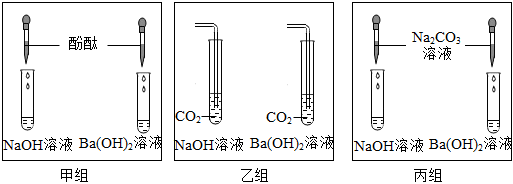
| 序号 | 操作 | 现象 | 结论 |
| 实验一 | 取滤液于试管中,滴加过量稀盐酸 | 猜想Ⅱ不成立 | |
| 实验二 | 取滤液于试管中,滴加几滴碳酸钠溶液 | 有白色沉淀生成 | 猜想Ⅲ成立 |
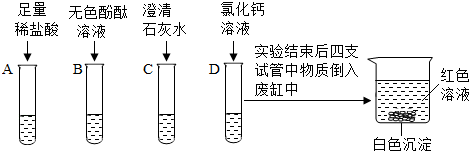
| 实验方案 | 实验现象 | 实验结论 | |
| 小田同学 | 取少量废液缸中上层红色溶液于试管中,加入过量的BaCl2溶液 | 观察到 | 猜想二成立 |
| 小威同学 | 取少量废液缸中上层红色溶液于试管中,加入过量的Ba(OH)2溶液 |

fik@dyw.com
2023-04-06
初中化学 | | 实验探究题