服务热线
搜题▪组卷
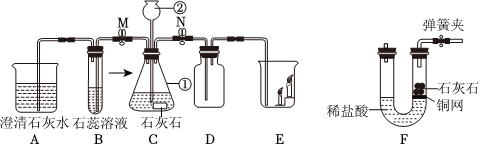 ?
?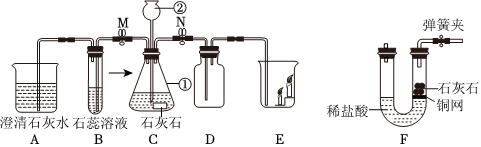 ?
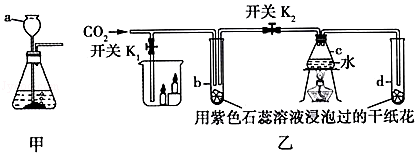
?
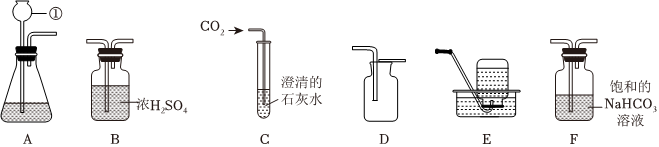
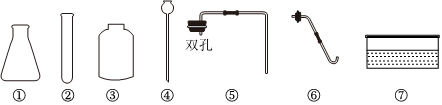
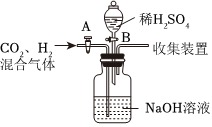
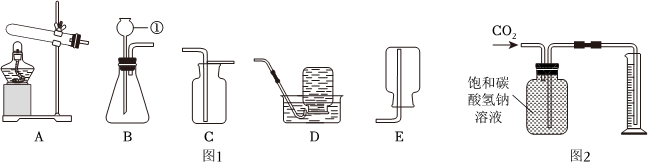
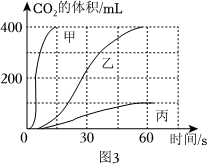
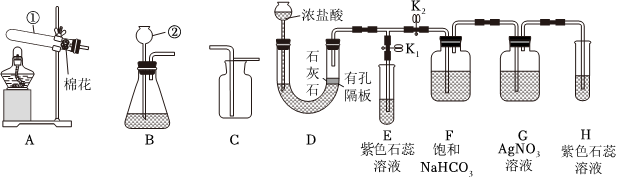
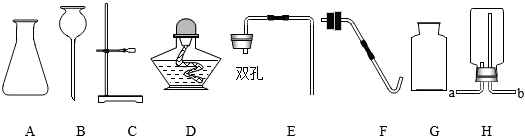
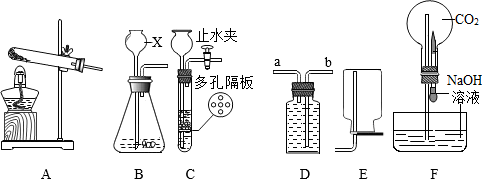
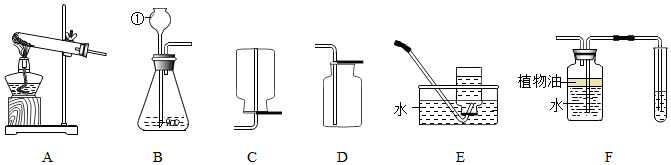
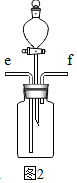
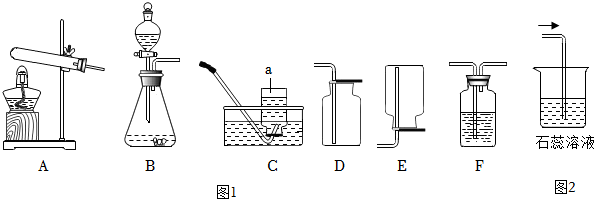
| 实验步骤 | 实验现象 | 实验结论 |
| 把镍浸入稀硫酸中 | (1) | 镍的活动性比氢强 |
| 把镍浸入硫酸亚铁溶液中 | 无明显现象 | 镍的活动性比铁(2) |
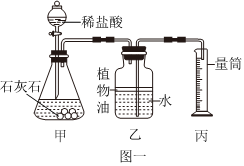
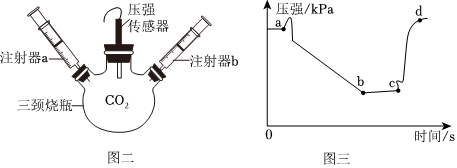

dm@dyw.com
2024-04-19
初中化学 | | 实验探究题