服务热线
搜题▪组卷
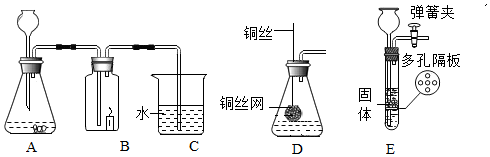
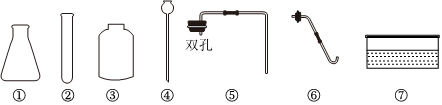
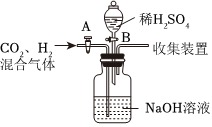
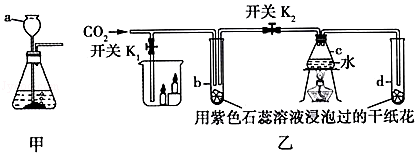
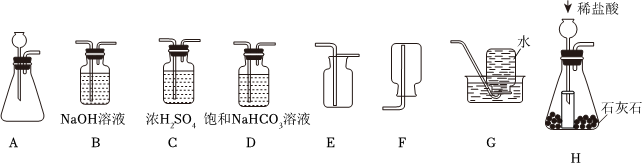
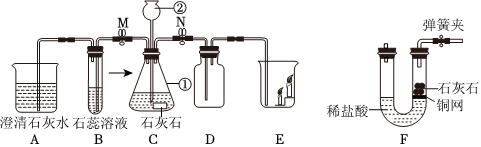 ?
? 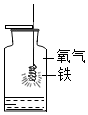 |
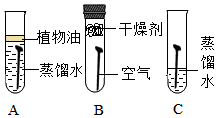 |
 |
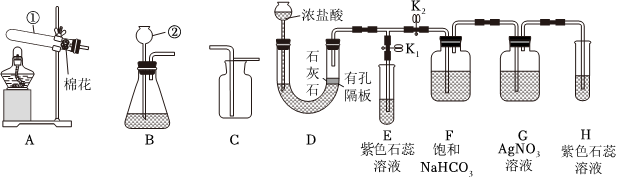
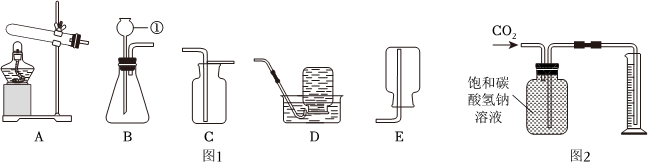
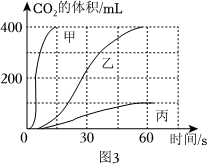
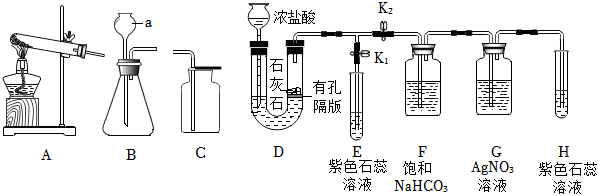
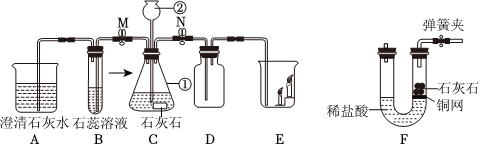
| 实验① | 实验② | 实验③ |
 ?
?
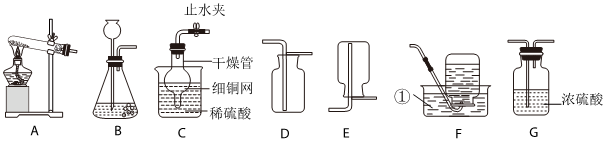
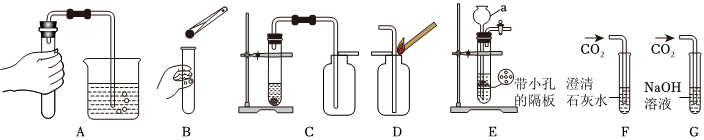
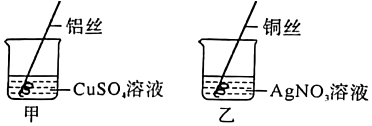
| 序号 | 实验操作 | 实验现象 | 实验结论 |
| 实验1 | 取少量废液于试管中,加入 稀盐酸 溶液 | 无明显现象 | 废液中没有AgNO3 |
| 实验2 | 取少量废液于试管中,加入Ba(NO3)2溶液 | 产生白色沉淀 | 废液中含有未反应完的CuSO4 |

bkj@dyw.com
2014-12-26
初中化学 | 九年级上 | 实验探究题