[解析]
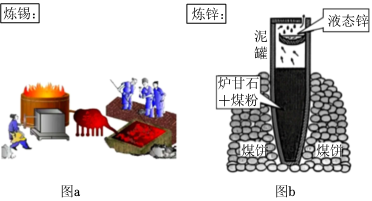
解:(1)为增大接触面积,充分反应,磁化铜矿焙烧前要进行粉碎处理;
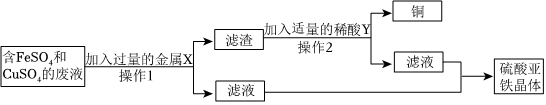
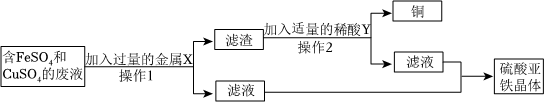
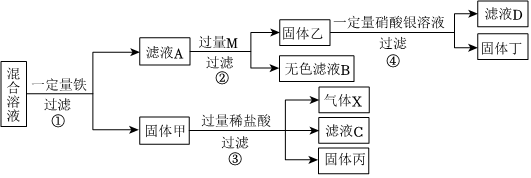
(2)据流程图可知,磁化铜矿焙烧生成黑色固体为氧化铜,氧化铜与硫酸反应得到硫酸铜溶液,即滤液,铁与硫酸铜反应生成铜和硫酸亚铁,化学方程式为Fe+CuSO4=FeSO4+Cu;
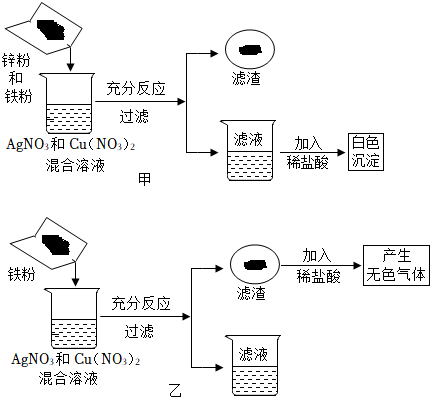
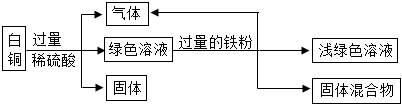
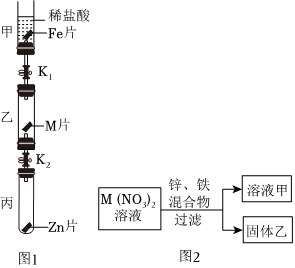
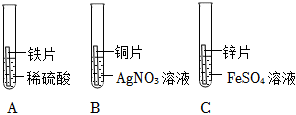
(3)A、甲中铁片与稀盐酸反应生成氯化亚铁溶液和氢气,氯化亚铁溶液是浅绿色溶液,所以甲中反应后得到浅绿色溶液,A不正确;
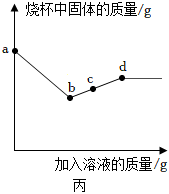
B、乙中无明显现象,说明金属活动性Fe>M,B正确;
C、Zn片表面变黑,即:
Zn+FeCl2=Fe+ZnCl2
127 136
根据化学方程式可知,136>127,所以丙中反应后溶液质量增大,C正确;
D、将M片和Zn片互换位置,乙中可得到Zn>Fe,丙中可得到Zn>M,不能比较Fe与M的活动性顺序,D不正确;
故选:BC;
(4)溶液甲是无色,说明铁没有与M(NO3)2溶液反应,锌与M(NO3)2溶液反应生成M和Zn(NO3)2溶液,则溶液甲一定含有Zn(NO3)2,溶液甲一定含有的金属阳离子是锌离子,符号为Zn2+。
故答案为:
(1)增大接触面积,充分反应;
(2)Fe+CuSO4=FeSO4+Cu;
(3)BC;
(4)Zn2+。



 ?
?