[答案]
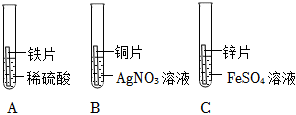
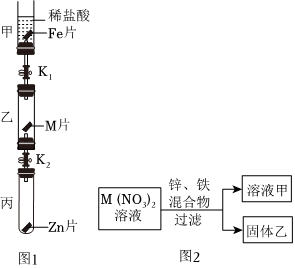
(1)产生气泡,溶液由无色逐渐变为浅绿色;
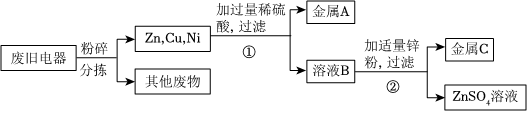
(2)Cu+2AgNO3=2Ag+Cu(NO3)2或Zn+FeSO4=Fe+ZnSO4;
(3)AC;
(4)不能。
[解析]
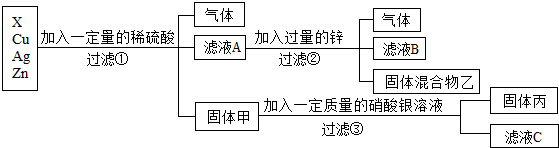
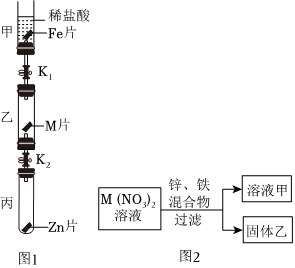
解:(1)A试管中铁片与稀盐酸反应生成氯化亚铁和氢气,故实验现象为:产生气泡,铁片逐渐溶解,溶液由无色变为浅绿色;
(2)试管B中铜片与硝酸银反应生成银和硝酸铜,发生反应的化学方程式:Cu+2AgNO3=2Ag+Cu(NO3)2或试管C中锌片与硝酸亚铁反应生成铁和硝酸锌,发生反应的化学方程式:Zn+FeSO4=Fe+ZnSO4;
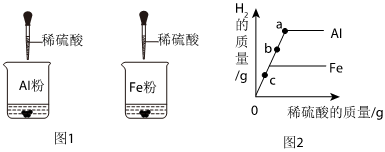
(3)试管A中铁和稀硫酸反应生成硫酸亚铁和氢气,反应后溶液质量变大,试管B中铜片与硝酸银反应生成银和硝酸铜,反应后溶液质量变小,试管C中锌片与硝酸亚铁反应生成铁和硝酸锌,反应后溶液质量变大;
(4)图A可知证明铁比氢活泼,图B可以证明铜比银活泼,图C可证明锌比铁活泼,但无法证明铁、铜的活动性,故无法判断金属活动性强弱;
故答案为:(1)产生气泡,溶液由无色逐渐变为浅绿色;
(2)Cu+2AgNO3=2Ag+Cu(NO3)2或Zn+FeSO4=Fe+ZnSO4;
(3)AC;
(4)不能。
[点评]
本题考查了"金属的化学性质,",属于"常考题",熟悉题型是解题的关键。


 ?
?