[解析]
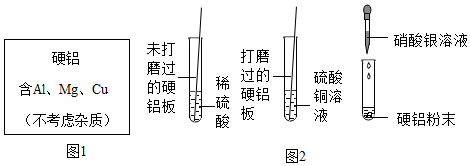
解:(1)将未打磨过的硬铝放入足量稀硫酸中,氧化铝先与盐酸反应生成氯化铝和水,然后铝、镁再与盐酸反应生成氢气,故整个过程中的实验现象是先无气泡产生,后有大量气泡产生,故选A。
(2)将打磨过硬铝片放入硫酸铜溶液中,镁与硫酸铜反应生成铜和硫酸镁,铝与硫酸铜反应生成硫酸铝和铜,化学反应的方程式分别为 CuSO4+Mg=MgSO4+Cu,2Al+3CuSO4═Al2(SO4)3+3Cu。
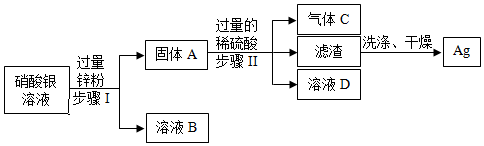
(3)将一定量硝酸银溶液滴入盛放有硬铝粉末的试管中,镁先与硝酸银反应生成银和硝酸镁,然后铝再与硝酸银反应生成银和硝酸铝,最后铜与硝酸银反应生成银和硝酸铜,充分反应后,过滤,得到滤渣和滤液。滤渣中加入稀盐酸无气泡产生,说明镁和铝已完全反应,铜可能反应,则滤渣中一定含有的金属是银,可能有铜。
故答案为:(1)A;(2)CuSO4+Mg=MgSO4+Cu或2Al+3CuSO4═Al2(SO4)3+3Cu;
(3)Ag。
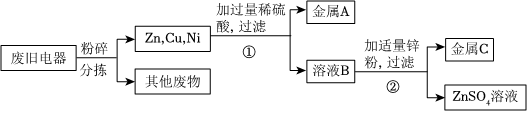



 ?
?