[解析]
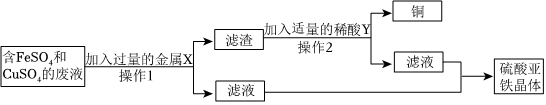
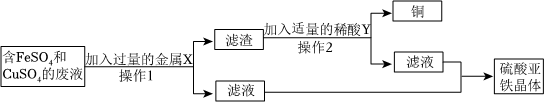
解:(1)操作1和操作2均是将不溶物质从溶液中分离的操作,为过滤操作,玻璃棒的作用是引流。
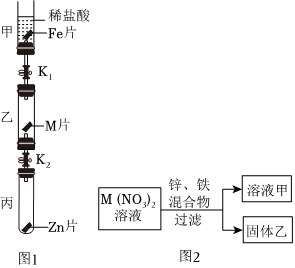
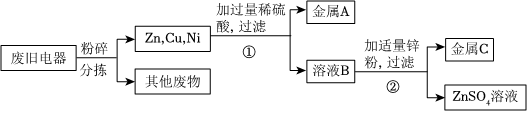
(2)小轩想从废液桶中的废液中回收金属铜和硫酸亚铁晶体,加入的过量的金属X为Fe,铁能与废液中的硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu。
(3)过滤后得到的滤渣为过量的铁和生成的铜的混合物,滤液为硫酸亚铁溶液;滤渣为铁、铜的混合物,加入适量的稀酸Y,铜不与Y反应,铁与Y反应,得到的滤液为硫酸亚铁溶液,则加入的稀酸Y为稀硫酸。铁与稀硫酸反应生成硫酸亚铁和氢气,则可以观察到有气泡产生,溶液颜色由无色变为浅绿色;经过操作2过滤后得到的滤液为硫酸亚铁溶液,其中含有的阳离子为Fe2+。
故答案为:
(1)引流;
(2)Fe+CuSO4═FeSO4+Cu;
(3)有气泡产生,溶液颜色由无色变为浅绿色;Fe2+。


 ?
?