[考点]
碱的化学性质,物质的鉴别、推断,书写化学方程式、文字表达式、电离方程式,
[答案]
(1)①;
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)H2O或CaCl2;HCl;
(4)A。
[解析]
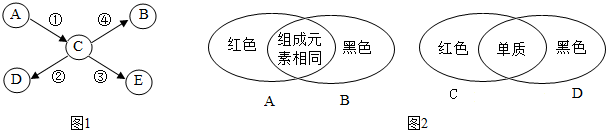
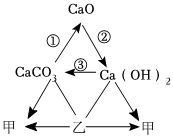
解:(1)工业上常用煅烧碳酸钙制取二氧化碳,反应序号①;
(2)实现反应③氢氧化钙转化成碳酸钙的复分解反应的方程式:氢氧化钙与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)乙能和碳酸钙反应、也能和氢氧化钙反应,所以乙是酸,可以是HCl,碳酸钙、氢氧化钙都能转换成甲,所以甲是氯化钙或者是水,乙和氢氧化钙溶液反应都能转化成甲,代入反应关系式,推导合理;甲、乙都由两种元素组成,甲、乙的化学式依次为CaCl2、HCl;
(4)A、碳在氧气不充足的条件下反应生成一氧化碳,碳在氧气充足的条件下反应生成二氧化碳,一氧化碳与氧气充分反应生成二氧化碳,二氧化碳与碳在高温条件下反应生成一氧化碳,含碳元素的物质通过一步转化可实现的“碳三角”关系图;
B、碳酸钙与稀盐酸反应生成二氧化碳、氯化钙和水,二氧化碳与氢氧化钙溶液反应生成碳酸钙沉淀和水,二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,碳酸钠与稀盐酸反应生成二氧化碳、水和氯化钠、碳酸钠和氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,碳酸钙不能转化成碳酸钠,含碳元素的物质通过一步转化不能完全实现的“碳三角”关系图;
故选:A。
故答案为:(1)①;
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)H2O或CaCl2;HCl;
(4)A。
[点评]
本题考查了"碱的化学性质,物质的鉴别、推断,书写化学方程式、文字表达式、电离方程式,",属于"典型题",熟悉题型是解题的关键。

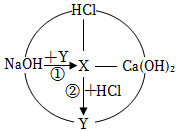 如图是初中常见物质的反应关系,其中X俗称苏打,“→”表示某物质可一步反应生成另一种物质,“—”表示两端的物质能相互反应(部分生成物已略去)。回答下列问题。
如图是初中常见物质的反应关系,其中X俗称苏打,“→”表示某物质可一步反应生成另一种物质,“—”表示两端的物质能相互反应(部分生成物已略去)。回答下列问题。