[考点]
碱的化学性质,盐的化学性质,物质的鉴别、推断,书写化学方程式、文字表达式、电离方程式,
[答案]
(1)过滤;
(2)BaCO3;
(3)2NaOH+Mg(NO3)2=2NaNO3+Mg(OH)2↓;
(4)NaCl、NaNO3;
(5)BaCl2、Mg(NO3)2、NaOH。
[解析]
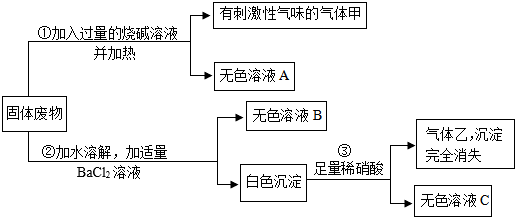
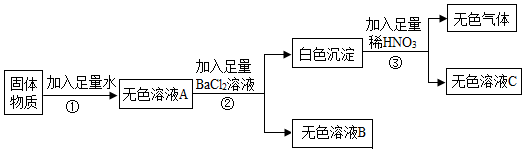
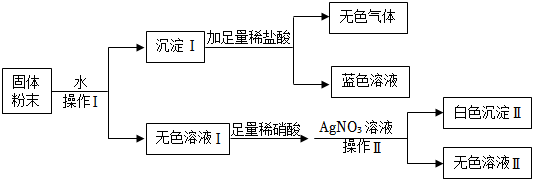
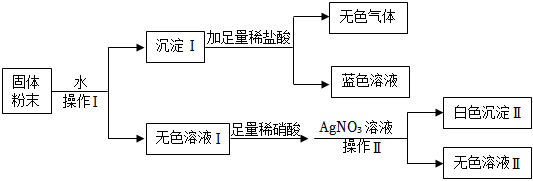
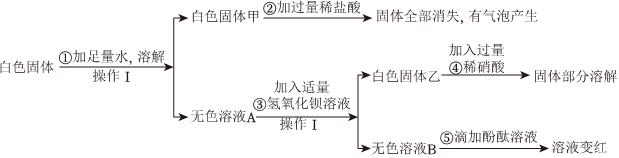
解:硫酸铜在溶液中显蓝色,硫酸根离子和钡离子反应生成不溶于酸的硫酸钡沉淀,碳酸钡不溶于水,溶于酸,氢氧根离子和镁离子反应生成溶于酸的氢氧化镁沉淀,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成碳酸钡沉淀。
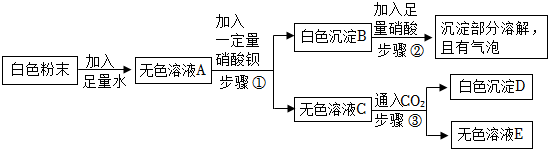
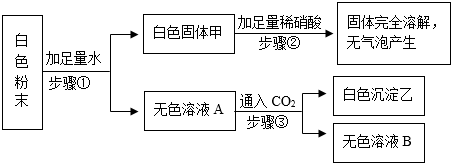
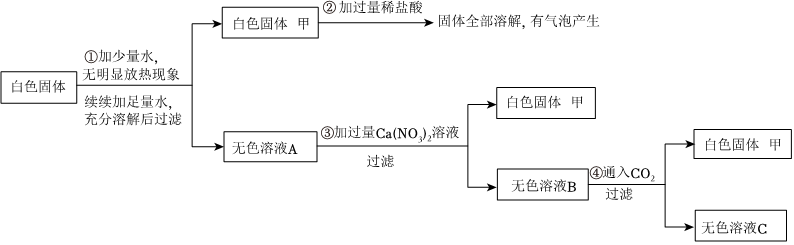
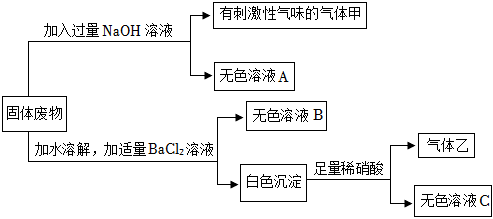
白色粉末溶于水得到无色溶液A和白色固体甲,说明原粉末中一定无CuSO4。白色固体甲加足量稀硝酸固体溶解但无气泡产生,说明沉淀不是碳酸盐沉淀,是氢氧化物沉淀,可以确定原粉末中一定无BaCO3,一定有Mg(NO3)2和NaOH,白色沉淀甲为Mg(OH)2。无色溶液A中通入CO2,有白色沉淀乙生成,说明溶液A中NaOH剩余,并还含有BaCl2,白色沉淀乙为BaCO3。在最终的无色溶液B中含有NaCl、NaNO3。
(1)白色粉末加入得到不溶性固体甲,用过滤的方法进行分离;
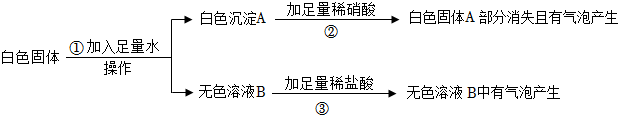
(2)根据步骤②的实验现象,可以确定原白色粉末中一定不含有BaCO3;
(3)白色固体甲是Mg(OH)2,氢氧化钠和硝酸镁反应生成氢氧化镁沉淀和硝酸钠,化学方程式为:2NaOH+Mg(NO 3)2=2NaNO3+Mg(OH)2↓;
(4)由上述分析可知,无色溶液B中一定含有的溶质是NaCl、NaNO3;
(5)根据前面的分析,可以确定原白色粉末中一定含有的物质是BaCl2、Mg(NO3)2、NaOH。
故答案为:(1)过滤;
(2)BaCO3;
(3)2NaOH+Mg(NO 3)2=2NaNO 3+Mg(OH)2↓;
(4)NaCl、NaNO3;
(5)BaCl2、Mg(NO3)2、NaOH。
[点评]
本题考查了"碱的化学性质,盐的化学性质,物质的鉴别、推断,书写化学方程式、文字表达式、电离方程式,",属于"综合题",熟悉题型是解题的关键。

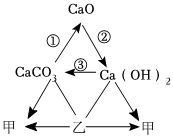

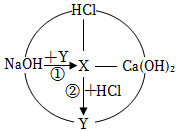 如图是初中常见物质的反应关系,其中X俗称苏打,“→”表示某物质可一步反应生成另一种物质,“—”表示两端的物质能相互反应(部分生成物已略去)。回答下列问题。
如图是初中常见物质的反应关系,其中X俗称苏打,“→”表示某物质可一步反应生成另一种物质,“—”表示两端的物质能相互反应(部分生成物已略去)。回答下列问题。