服务热线
搜题▪组卷
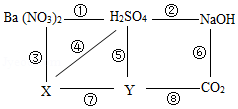
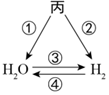
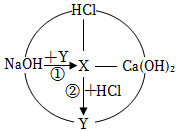 如图是初中常见物质的反应关系,其中X俗称苏打,“→”表示某物质可一步反应生成另一种物质,“—”表示两端的物质能相互反应(部分生成物已略去)。回答下列问题。
如图是初中常见物质的反应关系,其中X俗称苏打,“→”表示某物质可一步反应生成另一种物质,“—”表示两端的物质能相互反应(部分生成物已略去)。回答下列问题。
 |
 |
 |
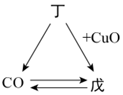 |
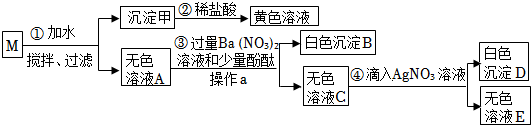
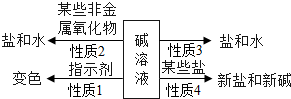
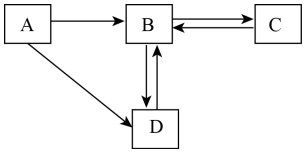
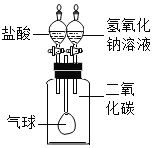
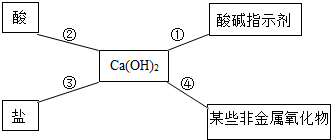
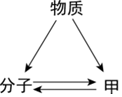
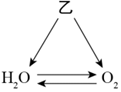
| (1)题图 | (2)题图 | (3)题图 | (4)题图 |
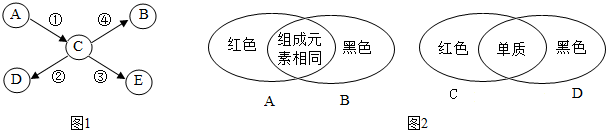
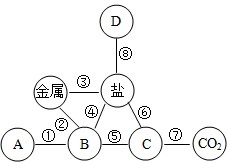
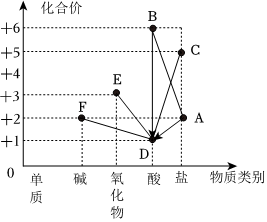 常见物质A→F中某种元素的化合价与物质类别的关系如图(“→”表示物质之间可以转化,“—”表示相连的物质能发生反应,部分反应物、生成物已省略)。其中D与E反应可清除铁制品表面的铁锈,F为蓝色固体。
常见物质A→F中某种元素的化合价与物质类别的关系如图(“→”表示物质之间可以转化,“—”表示相连的物质能发生反应,部分反应物、生成物已省略)。其中D与E反应可清除铁制品表面的铁锈,F为蓝色固体。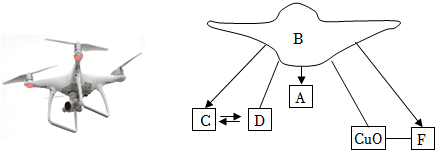

ty@dyw.com
2023-06-04
初中化学 | | 填空题