服务热线
搜题▪组卷

 |
 |
 |
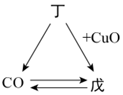 |
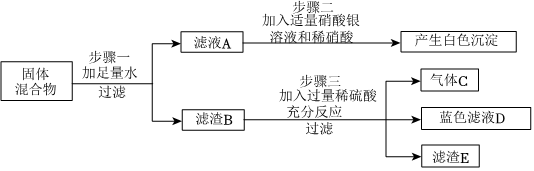
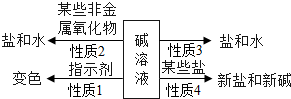
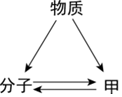
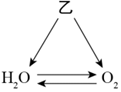
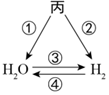
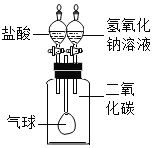
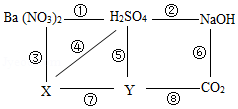
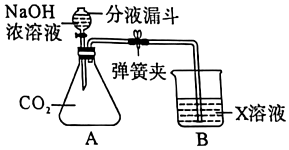
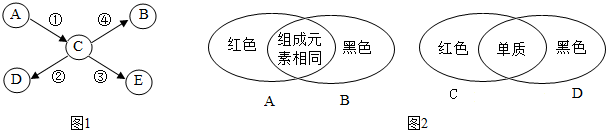
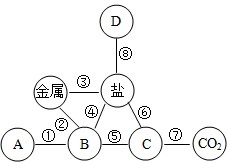
| (1)题图 | (2)题图 | (3)题图 | (4)题图 |
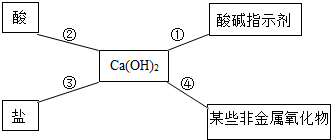
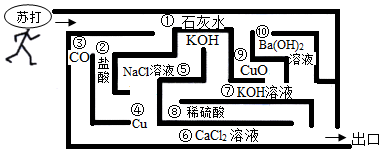
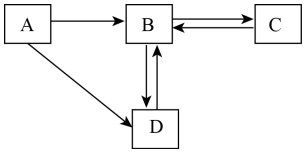
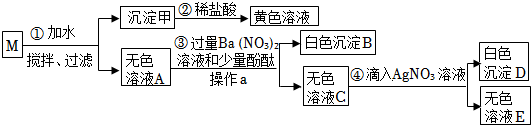


bjj@dyw.com
2013-04-15
初中化学 | | 填空题