[考点]
实验探究物质的组成成分以及含量,物质的性质决定的存放方式,生石灰的性质与用途,碱的化学性质,盐的化学性质,
[答案]
(1)2NaOH+CO2=Na2CO3+H2O;
(2)C;
(3)碳酸钙;
(4)氢氧化钠;有白色沉淀生成;过滤,再向滤液中加入无色酚酞溶液,氢氧化钠使酚酞变红;CD。
[解析]
(1)氢氧化钠久置在空气中会发生变质的反应为氢氧化钠和二氧化碳生成碳酸钠和水,化学方程式为2NaOH+CO2=Na2CO3+H2O。
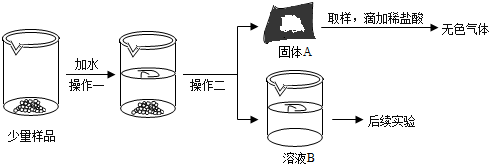
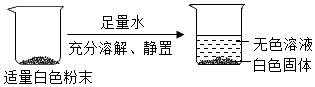
(2)氧化钙和水生成氢氧化钙,反应放热,氢氧化钠溶于水放热,同学们发现向样品中加水时放出大量的热,说明至少有CaO和NaOH中的一种。
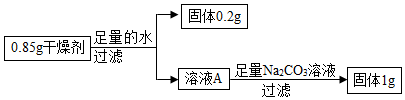
(3)碱石灰中氧化钙变质生成氢氧化钙或碳酸钙或两者都有,氢氧化钠变质生成碳酸钠,氢氧化钙溶液和碳酸钠溶液生成碳酸钙和氢氧化钠,经操作二将固液分离,为过滤操作,得到白色固体,则固体一定含有碳酸钙。
(4)样品加水,过滤得溶液B,结合以上分析,则溶液B的溶质可能是氢氧化钠,可能是碳酸钠,可能是氢氧化钠和碳酸钠,可能是氢氧化钙和氢氧化钠。
[实验验证]
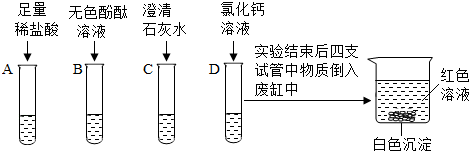
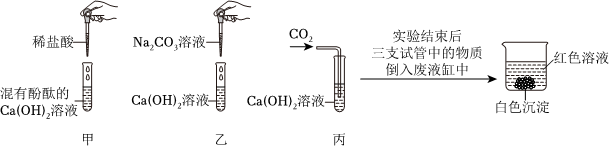
猜想三成立,则溶液B的溶质为氢氧化钠和碳酸钠,取少量溶液B于试管中,加入足量的氯化钙溶液,碳酸钠和氯化钙生成碳酸钙和氯化钠,有白色沉淀生成,过滤,再向滤液中加入无色酚酞溶液,氢氧化钠使酚酞变红。
[交流反思]
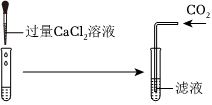
①CaCl2溶液检验除去碳酸钠。
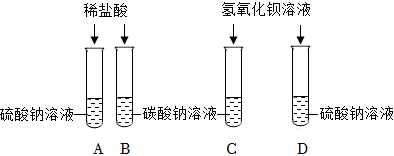
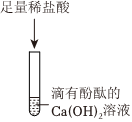
A、稀盐酸先和氢氧化钠反应,后和碳酸钠反应生成气体,能检验碳酸钠,但干扰溶液中氢氧化钠的检验,选项错误;
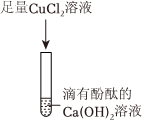
B、Ca(OH)2溶液和碳酸钠生成碳酸钙沉淀和氢氧化钠,能检验碳酸钠,但干扰溶液中氢氧化钠的检验,选项错误;
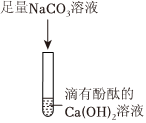
C、BaCl2溶液和碳酸钠生成碳酸钡沉淀和氯化钠,能检验碳酸钠,且不干扰溶液中氢氧化钠的检验,选项正确;
D、Ca(NO3)2 溶液和碳酸钠生成碳酸钙沉淀和氯化钠,能检验碳酸钠,且不干扰溶液中氢氧化钠的检验,选项正确。
故答案为:
(1)2NaOH+CO2=Na2CO3+H2O;
(2)C;
(3)碳酸钙;
(4)氢氧化钠;有白色沉淀生成;过滤,再向滤液中加入无色酚酞溶液,氢氧化钠使酚酞变红;CD。
[点评]
本题考查了"实验探究物质的组成成分以及含量,物质的性质决定的存放方式,生石灰的性质与用途,碱的化学性质,盐的化学性质,",属于"压轴题",熟悉题型是解题的关键。
 兴趣小组同学自制呼吸面具,准备用过氧化钠(Na2O2)作为供氧剂,但在实验室找到了一瓶敞口放置的过氧化钠。
兴趣小组同学自制呼吸面具,准备用过氧化钠(Na2O2)作为供氧剂,但在实验室找到了一瓶敞口放置的过氧化钠。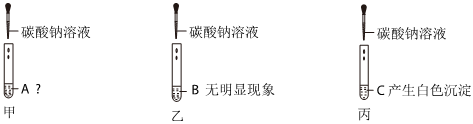
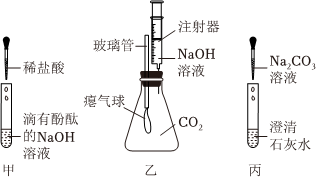
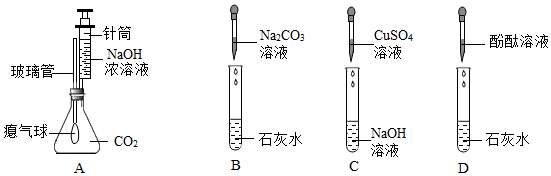
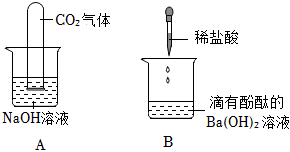 实验课上,某化学小组探究两个初中常见的无明显现象的反应:甲同学利用装置A将装满CO2的试管倒扣在盛有NaOH溶液的烧杯中,乙同学借助无色酚酞溶液利用装置B进行中和反应,如图所示:
实验课上,某化学小组探究两个初中常见的无明显现象的反应:甲同学利用装置A将装满CO2的试管倒扣在盛有NaOH溶液的烧杯中,乙同学借助无色酚酞溶液利用装置B进行中和反应,如图所示: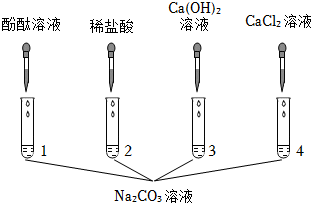 ?
?