[解析]
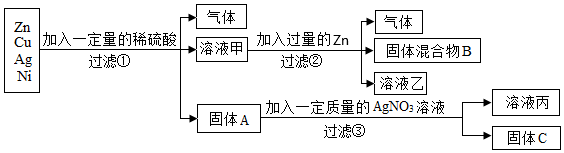
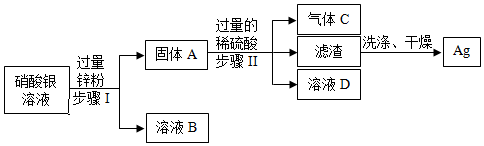
解:(1)Zn和稀硫酸反应生成硫酸锌和氢气,Ni和稀硫酸反应生成+2价化合物和氢气,铜、银不能和稀硫酸反应,②中加入过量的锌,产生气体,说明①中稀硫酸过量,则①中锌、镍完全反应,固体A的成分是铜、银,化学式为:Cu、Ag。
(2)②中加入过量的锌,得到固体混合物B,则B中含有锌和镍,说明锌比镍活泼,所以②中锌和硫酸镍反应生成硫酸锌和镍,反应的化学方程式:Zn+NiSO4=ZnSO4+Ni。
(3)在金属活动性顺序中,Zn>H>Cu>Ag,由以上过程可知,锌能和硫酸镍,说明锌的活动性强于镍,镍能和硫酸反应,说明在金属活动性顺序中,镍排在氢前面,则活动性顺序为:Zn>Ni>H,所以可以推测Zn、Cu、Ag、Ni四种金属的活动性从强到弱是:Zn>Ni>Cu>Ag。
(4)①锌、镍都能和硫酸铜反应,说明铜最不活泼,都是不能比较锌和镍的活泼性,故选项试剂不可行;
②铜、镍都不能和硫酸锌反应,说明锌最活泼,不能比较铜和镍的活泼性,故选项试剂不可行;
③锌能和硫酸镍反应,说明锌比镍活泼,铜不能和硫酸镍反应,说明镍比铜活泼,则Zn、Cu、Ni的活动性强弱顺序为:Zn>Ni>Cu,故选项试剂可行。
故选:③。
故答案为:
(1)Cu、Ag;
(2)Zn+NiSO4=ZnSO4+Ni;
(3)Zn>Ni>Cu>Ag;
(4)③。



 ?
?