[考点]
金属的化学性质,金属活动性顺序及其应用,
[答案]
(1)促进燃烧。
(2)速率。
(3)Fe+H2SO4═FeSO4+H2↑。
(4)Zn2+。
[解析]
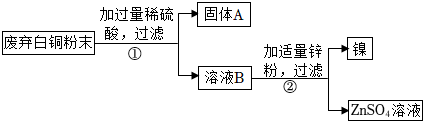
解:(1)鼓入足量空气的目的是促进燃烧,从而提高炉温。
故答案为:促进燃烧。
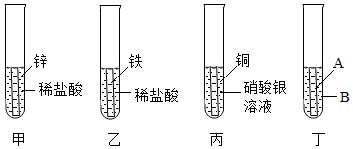
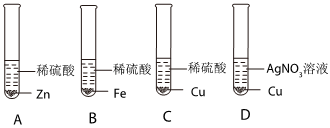
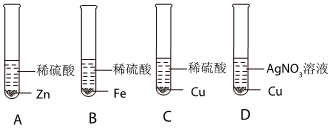
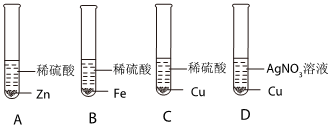
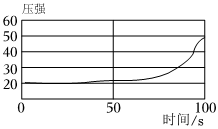
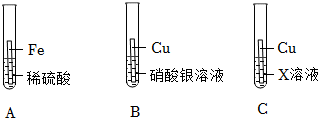
(2)小华设计了如图所示实验,可通过观察产生气泡的速率来比较锌和铁的活动性强弱。
故答案为:速率。
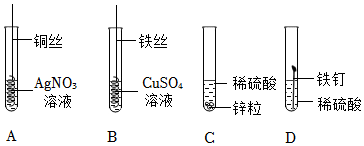
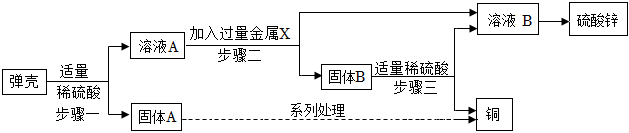
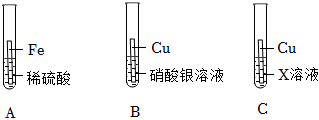
(3)试管B和C中能发生反应的化学方程式为Fe+H2SO4═FeSO4+H2↑。
故答案为:Fe+H2SO4═FeSO4+H2↑。
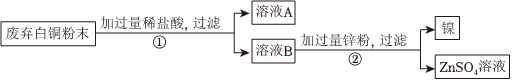
(4)同学们向D试管中继续加入锌粉和铁粉的混合物,充分反应后过滤,得到无色滤液,说明滤液中不含有亚铁离子和铜离子,则该滤液中含有的阳离子是锌离子。
故答案为:Zn2+。
[点评]
本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。


 ?
? ?
? ?
? ?
? ?
?