[考点]
合金与合金的性质,金属的化学性质,金属活动性顺序及其应用,
[答案]
(1)②④;
(2)铁和银;
(3)①Fe+2HCl═FeCl2+H2↑;
②硫酸铜(合理即可)。
[解析]
解:(1)①合金中不一定含有两种金属,故错误;
②合金是由不同种物质组成的,一定是混合物,故正确;
③合金中的元素主要以单质的形式存在,故错误;
④合金的硬度一般比组成它的纯金属更高,抗腐蚀性也更好,故正确;
⑤焊锡焊接金属利用了熔点低的特性,故错误。
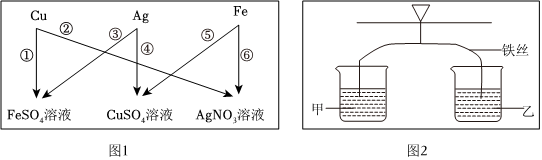
(2)由于金属的活动性是:锌比铁活泼,铁比银活泼,将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,锌先和硝酸银反应生成硝酸锌和银,如果锌不足,则铁再和硝酸银反应生成硝酸亚铁和银,由于充分反应后过滤,得到滤渣和滤液。将所得滤渣放入稀盐酸中,有气泡产生,说明了剩余的固体中一定有铁,还有置换出的银,则则滤渣中一定含有铁和银。
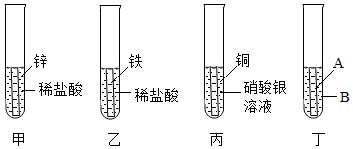
(3)①由题意可知,反应过程中溶液颜色变为浅绿色反应是铁与稀盐酸发生反应生成了氯化亚铁和氢气,化学反应方程式是:Fe+2HCl═FeCl2+H2↑。
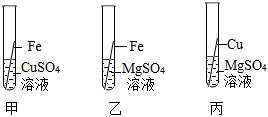
②通过甲、乙可以比较出锌比铁活泼,通过丁可以比较出铜比银活泼,但不能比较铁与铜的活泼性强弱,于是又补充图丁实验,最终得出四种金属活动性顺序为:Zn>Fe>Cu>Ag,若A为金属铁,则试剂B为硫酸铜等溶液。
故答案为:(1)②④;
(2)铁和银;
(3)①Fe+2HCl═FeCl2+H2↑;
②硫酸铜(合理即可)。
[点评]
本题考查了"合金与合金的性质,金属的化学性质,金属活动性顺序及其应用,",属于"难典题",熟悉题型是解题的关键。
 ?
?


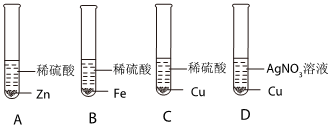
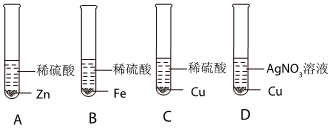
 实验中一个能发生反应的化学方程式 。
实验中一个能发生反应的化学方程式 。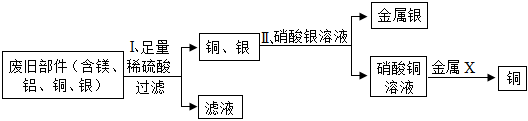
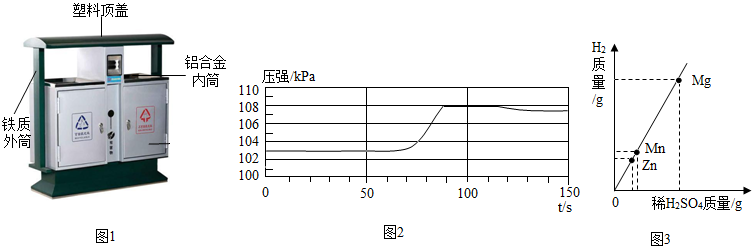 (1)空易拉罐应放入 (选填可回收物或其它垃圾)筒中。
(1)空易拉罐应放入 (选填可回收物或其它垃圾)筒中。