[考点]
溶液的概念、组成及其特点,溶解时的吸热或放热现象,饱和溶液和不饱和溶液,饱和溶液和不饱和溶液相互转变的方法,晶体和结晶的概念与现象,固体溶解度曲线及其作用,溶质的质量分数,
[答案]
(1)B;
(2)加水;
(3)=;
(4)B;
(5)C。
[解析]
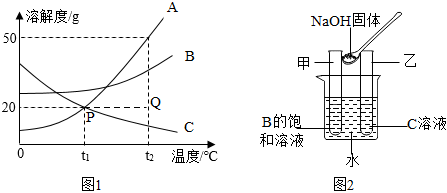
解:(1)A、氢氧化钠固体溶于水放出热量,溶液的温度会升高,不合题意;
B、硝酸铵固体溶于水吸收热量,溶液的温度会降低,符合题意;
C、氯化钠固体溶于水温度几乎不变,不合题意;
D、蔗糖固体溶于水温度几乎不变,不合题意;
故答案为:B;
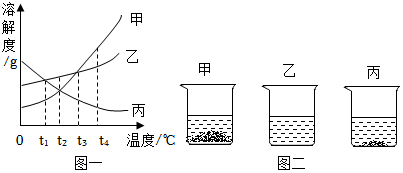
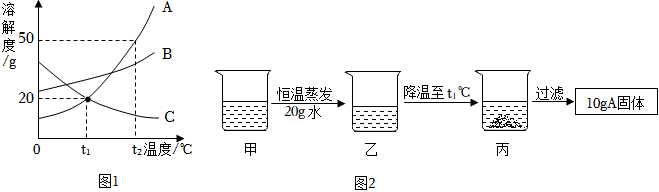
(2)由溶解度曲线可知,甲和乙的溶解度都是随着温度的升高而增大,而丙的溶解度是随着温度的升高而减小,因此能同时使甲、乙、丙三种物质的饱和溶液变为不饱和溶液的方法是只能采取加溶剂的方法;故答案为:加水;
(3)由溶解度曲线可知,t1℃时乙、丙两种物质的溶解度相等,因此将等质量的乙、丙两种物质分别加水配成t1℃时的饱和溶液,所得溶液的质量乙等于丙;故答案为:=;
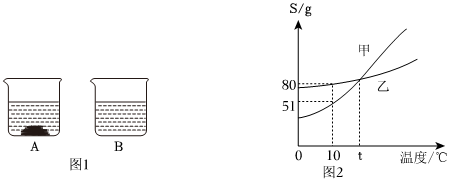
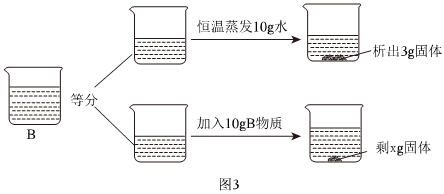
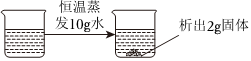
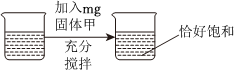
(4)20℃时,把等质量的甲、乙、丙三种固体分别加入到盛有50g水的烧杯中,充分溶解后,所得现象如图2,分析可知,20℃时,三种物质的溶解度大小为乙>丙>甲,由图象可知:20℃所处的温度范围是t1<20<t2;故答案为:B;
(5)由溶解度曲线可知,甲的溶解度都是随着温度的升高而增大,而丙的溶解度是随着温度的升高而减小。因此将等质量甲、丙的饱和溶液从t4℃降温到t2℃,甲中有晶体析出,溶液仍为饱和状态,丙中没有析出晶体,溶液变成不饱和状态。
A、甲仍为饱和溶液,而丙变成了不饱和溶液,故A错误;
B、甲中有晶体析出,溶液的质量减小,而丙溶液的质量不变,因此溶液的质量甲<丙,故B错误;
C、t4℃时,甲的溶解度大于丙,因此该温度下等质量甲、丙的饱和溶液中,丙的饱和溶液中所含溶剂多,而降温过程中,溶剂的质量不变,因此溶剂的质量甲<丙,故C正确;
D、从t4℃降温到t2℃,甲仍为饱和溶液,而丙变成了不饱和溶液,但溶液中溶质的质量分数没有改变,由溶解度曲线可知,t2℃时,甲的溶解度大于t4℃时丙的溶解度,因为某温度下的饱和溶液中,溶质的质量分数= ,因此,从t4℃降温到t2℃,溶质的质量分数甲>丙,故D错误。
故答案为:C。
,因此,从t4℃降温到t2℃,溶质的质量分数甲>丙,故D错误。
故答案为:C。
[点评]
本题考查了"溶液的概念、组成及其特点,溶解时的吸热或放热现象,饱和溶液和不饱和溶液,饱和溶液和不饱和溶液相互转变的方法,晶体和结晶的概念与现象,固体溶解度曲线及其作用,溶质的质量分数,",属于"压轴题",熟悉题型是解题的关键。
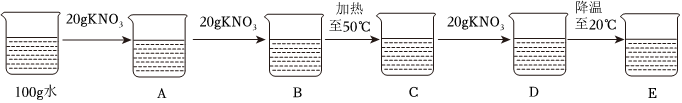
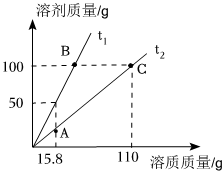 硝酸钾在不同温度下的溶解度如表所示,据此画出不同温度下硝酸钾在溶解时恰好达到饱和状态时溶质质量与溶剂质量的关系。
硝酸钾在不同温度下的溶解度如表所示,据此画出不同温度下硝酸钾在溶解时恰好达到饱和状态时溶质质量与溶剂质量的关系。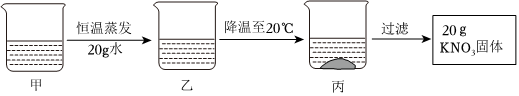
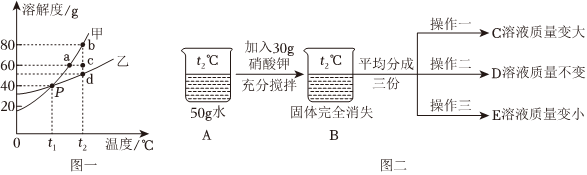
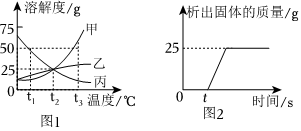
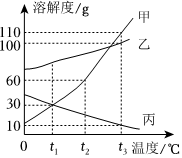
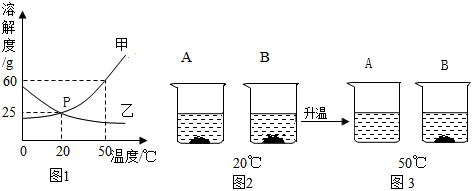
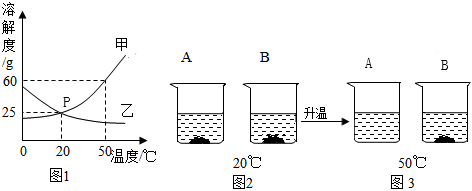
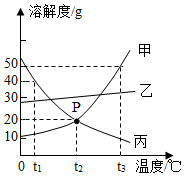 如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线.请根据图回答:
如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线.请根据图回答: