服务热线
搜题▪组卷
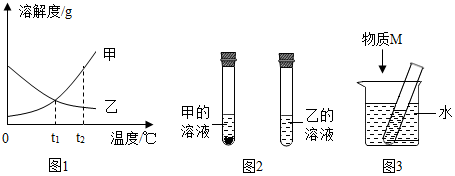
| 选项 | A | B | C | D |
| 试管内溶液中的溶质 | 甲 | 乙 | 甲 | 乙 |
| 物质M | NaOH | NaOH | NaCl | NH4NO3 |
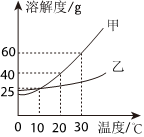 如图是甲、乙两种固体物质的溶解度曲线。据图回答:
如图是甲、乙两种固体物质的溶解度曲线。据图回答: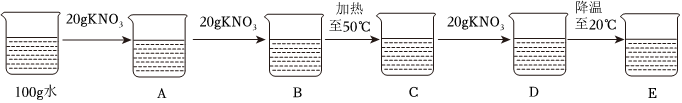
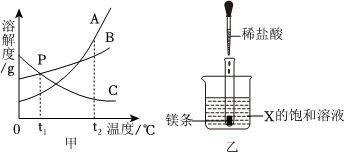
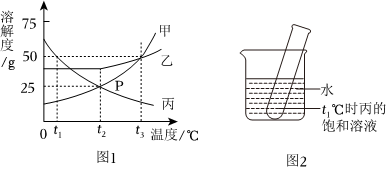
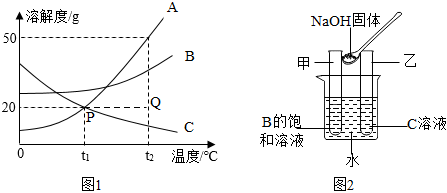
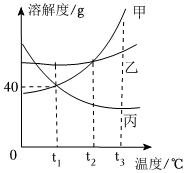
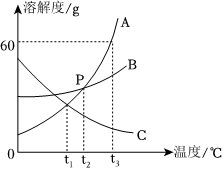
 如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答下列问题。
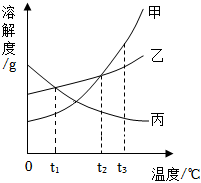
如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答下列问题。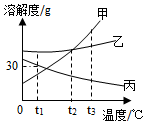 如图是甲、乙、丙三种固体物质(受热均不分解,且晶体均不含结晶水)在水中的溶解度曲线。请据图回答下列问题:
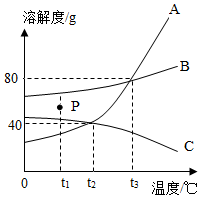
如图是甲、乙、丙三种固体物质(受热均不分解,且晶体均不含结晶水)在水中的溶解度曲线。请据图回答下列问题:
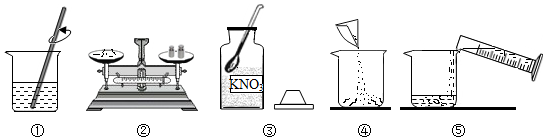
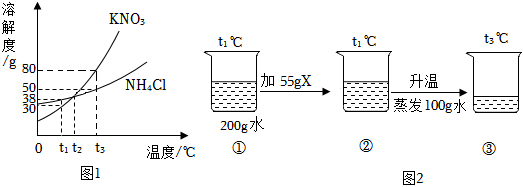
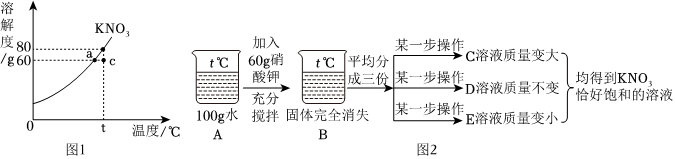
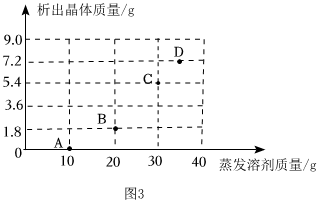
 甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答下列问题。
甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答下列问题。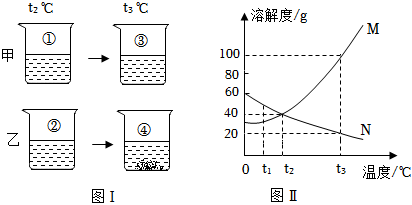
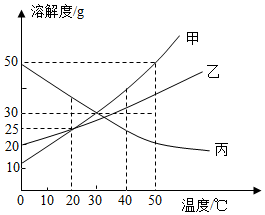
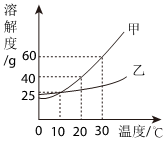 如图是甲、乙两种固体物质的溶解度曲线。据图回答:?
如图是甲、乙两种固体物质的溶解度曲线。据图回答:?
lch@dyw.com
2022-04-15
初中化学 | | 填空题