[考点]
金属与酸的反应原理,金属与盐溶液反应的原理,物质的相互转化和制备,
[答案]
(1)玻璃棒;
(2)Fe、Cu;
(3)Zn+2AgNO3=Zn(NO3)2+2Ag;ACD。
[解析]
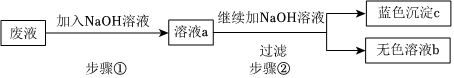
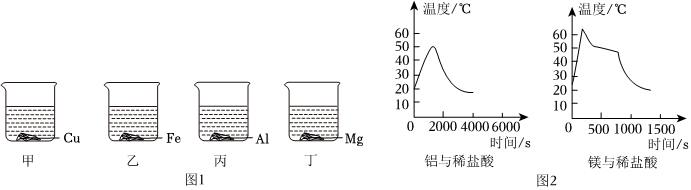
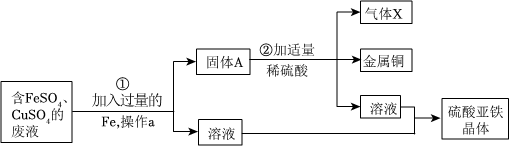
解:(1)操作a实现了固液分离,是过滤操作。如图所示,过滤所需的玻璃仪器除了漏斗、烧杯之外,还需要玻璃棒;
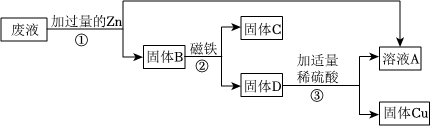
(2)向废液中加入过量的铁,铁和硫酸铜反应生成硫酸亚铁和铜,反应方程式为Fe+CuSO4=FeSO4+Cu。所以固体A中含有过量的铁和生成的铜,其化学式为Fe、Cu;
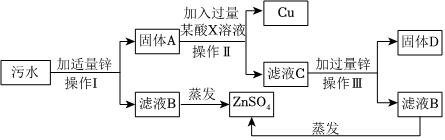
(3)金属活动性顺序为Zn>Cu>Ag,含硝酸银、硝酸铜的混合废液,向其中加入一定量锌粉,锌先与硝酸银反应生成硝酸锌和银,待硝酸银完全反应后,锌和硝酸铜反应生成硝酸锌和铜。反应停止后过滤,滤液仍为蓝色,说明滤液中含硝酸铜,则锌已经完全反应;锌首先置换银,反应的化学方程式为Zn+2AgNO3=Zn(NO3)2+2Ag;
A.由分析可知,锌已经完全反应,锌一定与硝酸银反应生成了银,则滤渣中一定含银,可能含铜,故正确;
B.将滤渣加入稀盐酸中,铜、银和稀盐酸均不反应,均无明显现象,B错误;
C.锌一定与硝酸银反应生成了硝酸锌,由分析可知,滤液中一定含硝酸铜,则滤液中一定含硝酸锌、硝酸铜,可能含硝酸银,C正确;
D.由分析可知,反应停止后过滤,滤液仍为蓝色;可能是锌置换出部分银,硝酸银溶液有剩余;D正确;
故选:ACD。
故答案为:
(1)玻璃棒;
(2)Fe、Cu;
(3)Zn+2AgNO3=Zn(NO3)2+2Ag;ACD。
[点评]
本题考查了"金属与酸的反应原理,金属与盐溶液反应的原理,物质的相互转化和制备,",属于"难典题",熟悉题型是解题的关键。
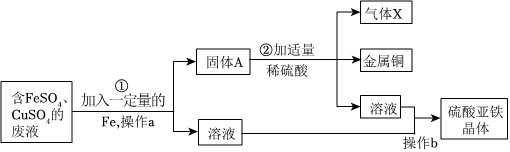
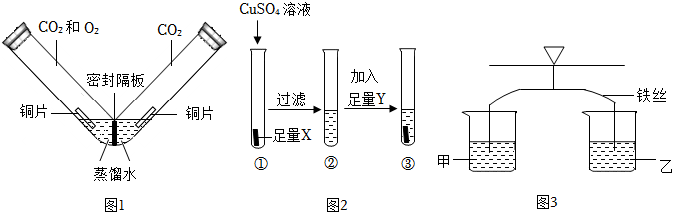
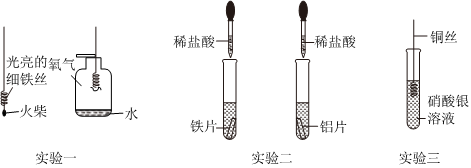
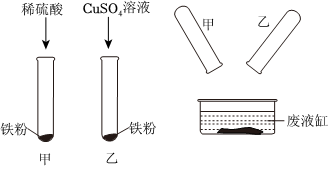
 人类文明的发展和社会的进步与金属材料的关系十分密切。如图是有关金属的实验,请结合金属的相关知识分析以下问题。
人类文明的发展和社会的进步与金属材料的关系十分密切。如图是有关金属的实验,请结合金属的相关知识分析以下问题。