[考点]
金属活动性强弱的判断,物质的相互转化和制备,
[答案]
(1)Zn+CuSO4=ZnSO4+Cu或Zn+FeSO4=ZnSO4+Fe;
(2)Zn、Fe、Cu;
(3)C。
[解析]
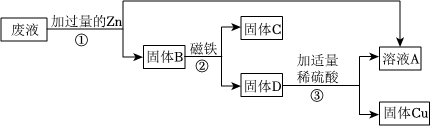
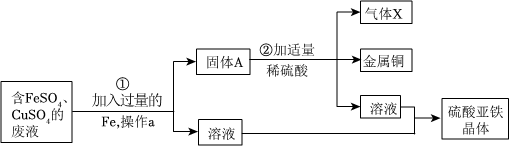
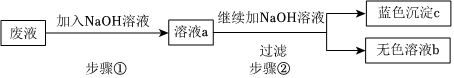
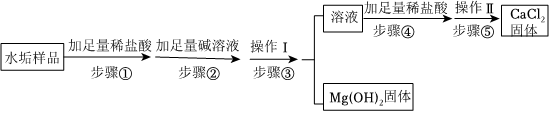
解:(1)根据金属活动性顺序表:Zn>Fe>Cu,排在前面的金属一般能把排在后面的金属从其盐溶液里置换出来;所以,向废液中加入过量的锌粉,步骤①中发生的化学反应化学方程式是Zn+CuSO4=ZnSO4+Cu;Zn+FeSO4═ZnSO4+Fe;
(2)由以上分析知,向混合溶液中加入过量锌粉后,锌先和硫酸铜反应,后和硫酸亚铁反应,所得固体的组成:锌、铁、铜。
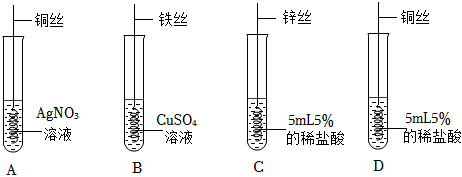
(3)A.产生气泡速率快的是锌,产生气泡速率慢的是铁,无气泡产生的是铜,可以证明了三种金属的活动性顺序:锌>铁>铜,故正确;
B.铁能和硫酸铜溶液反应,不能和硫酸锌溶液反应,可以证明了三种金属的活动性顺序:锌>铁>铜,故正确;
C.铁片、锌片均与硫酸铜溶液反应,只能证明铁、锌比铜活泼,不能得出锌、铁的金属活动性强弱,故错误。
故选:C。
故答案为:
(1)Zn+CuSO4=ZnSO4+Cu或Zn+FeSO4=ZnSO4+Fe;
(2)Zn、Fe、Cu;
(3)C。
[点评]
本题考查了"金属活动性强弱的判断,物质的相互转化和制备,",属于"必考题",熟悉题型是解题的关键。
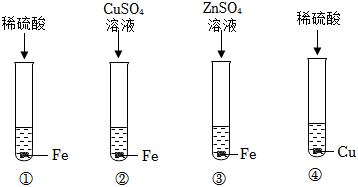
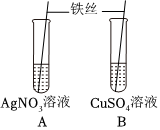 铁是生活中常见的金属,某同学用打磨过的铁丝进行如图实验。
铁是生活中常见的金属,某同学用打磨过的铁丝进行如图实验。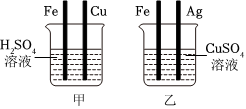
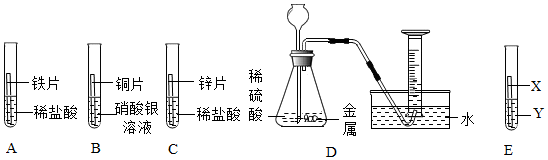
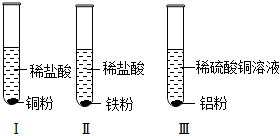
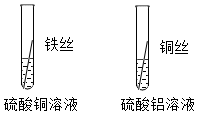 铁、铜、铝是生活中最常用的三种金属,小圆同学选取实验室提供的铁、铜、铝、稀硫酸、硫酸铜溶液、硫酸铝溶液,做了以下实验:
铁、铜、铝是生活中最常用的三种金属,小圆同学选取实验室提供的铁、铜、铝、稀硫酸、硫酸铜溶液、硫酸铝溶液,做了以下实验: