[解析]
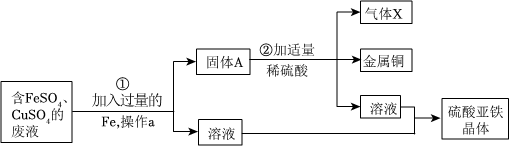
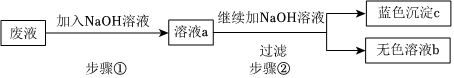
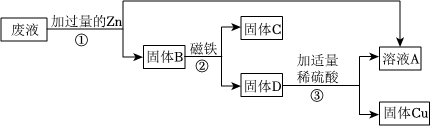
解:向FeSO4、CuSO4的废液加入过量的Fe,Fe与CuSO4反应生成FeSO4和Cu,所以固体A是剩余的Fe和置换出来的Cu,此时溶液中的成分是FeSO4,向固体A中加入适量稀硫酸,Fe与稀硫酸反应生成FeSO4和氢气,所以气体X是氢气,此时溶液中的成分是FeSO4,故从溶液中可回收硫酸亚铁晶体;
(1)通过操作a将固体和溶液分离,所以操作a是过滤;故答案为:过滤;
(2)铁会与硫酸铜反应生成硫酸亚铁和铜,加入过量Fe的目的是将硫酸铜中的铜全部置换出来,加入Fe的量不足,可能造成的结果是不能将铜全部置换出来,得不到纯净的硫酸亚铁溶液;故答案为:不能将铜全部置换出来,得不到纯净的硫酸亚铁溶液;
(3)由分析可知,固体A是剩余的Fe和置换出来的Cu;故答案为:Fe和Cu;
(4)②步骤是铁和硫酸反应生成氢气和硫酸亚铁,化学方程式为:H2SO4+Fe=FeSO4+H2↑;故答案为:H2SO4+Fe=FeSO4+H2↑。