[答案]
(1)出现较多固体;
(2)将氯化镁、硫酸钠完全转化为沉淀除去;
(3)Na2CO3+CaCl2=CaCO3↓+2NaCl或Na2CO3+BaCl2=BaCO3↓+2NaCl或Ba(OH)2+Na2CO3=BaCO3↓+2NaOH。
[解析]
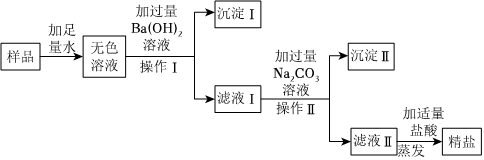
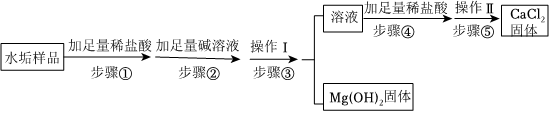
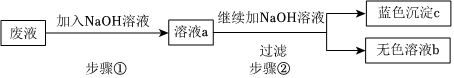
解:样品加足量水溶解得到无色溶液,该溶液中含有氯化钠、氯化钙、氯化镁和硫酸钠,加过量氢氧化钡溶液,氢氧化钡与氯化镁反应生成氢氧化镁沉淀和氯化钡,硫酸钠与氢氧化钡反应生成硫酸钡沉淀和氢氧化钠,充分反应后过滤得到滤液Ⅰ,滤液Ⅰ中含有氯化钠、氯化钙、氢氧化钠、氯化钡和氢氧化钡,加过量碳酸钠溶液,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,碳酸钠与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,充分反应后过滤得到滤液Ⅱ,滤液Ⅱ中含有氯化钠、氢氧化钠和碳酸钠,加适量盐酸,盐酸与氢氧化钠反应生成氯化钠和水,盐酸与碳酸钠反应生成氯化钠、二氧化碳和水,充分反应后得到氯化钠溶液,蒸发得到精盐;
(1)进行蒸发操作时,当蒸发皿中出现较多固体时,停止加热,利用余热使滤液蒸干;故答案为:出现较多固体;
(2)由分析可知,加入过量Ba(OH)2溶液的目的是将氯化镁、硫酸钠完全转化为沉淀除去;故答案为:将氯化镁、硫酸钠完全转化为沉淀除去;
(3)向滤液Ⅰ中加入的Na2CO3溶液,发生反应的化学方程式为碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,碳酸钠与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl、Na2CO3+BaCl2=BaCO3↓+2NaCl、Ba(OH)2+Na2CO3=BaCO3↓+2NaOH;故答案为:Na2CO3+CaCl2=CaCO3↓+2NaCl或Na2CO3+BaCl2=BaCO3↓+2NaCl或Ba(OH)2+Na2CO3=BaCO3↓+2NaOH。
[点评]
本题考查了"物质的相互转化和制备,",属于"基础题",熟悉题型是解题的关键。