[答案]
(1)引流;
(2)Zn+CuSO4=ZnSO4+Cu或Zn+FeSO4=ZnSO4+Fe;
(3)有气泡产生;
(4)增大。
[解析]
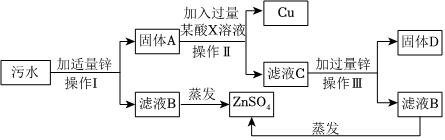
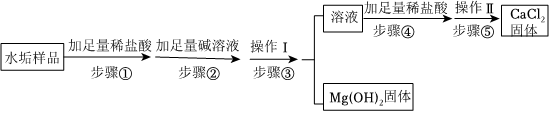
解:(1)操作Ⅰ、Ⅱ、Ⅲ都是将固体和液体分离的操作,即过滤操作。在过滤操作中,玻璃棒的作用是引流,防止液体洒出;
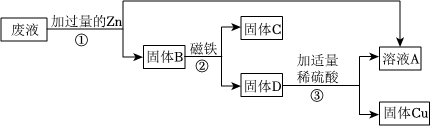
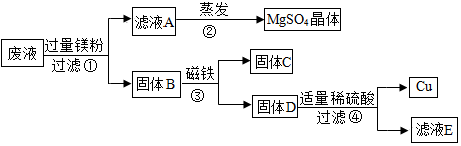
(2)污水中含有CuSO4、FeSO4和ZnSO4,加入过量锌,锌的金属活动性比铜和铁强,会发生置换反应。锌与硫酸铜反应的化学方程式为Zn+CuSO4=ZnSO4+Cu;锌与硫酸亚铁反应的化学方程式为Zn+FeSO4=ZnSO4+Fe;
(3)固体A是锌、铜、铁的混合物,加入某酸X溶液后,锌和铁会与酸反应。因为有固体减少,说明锌和铁在与酸反应,同时会产生氢气,所以现象是有气泡产生;
(4)在整个过程中,加入了过量的锌,锌与硫酸铜、硫酸亚铁反应都生成了硫酸锌,所以最终得到的ZnSO4较污水中原有ZnSO4质量增大。
故答案为:
(1)引流;
(2)Zn+CuSO4=ZnSO4+Cu或Zn+FeSO4=ZnSO4+Fe;
(3)有气泡产生;
(4)增大。
[点评]
本题考查了"物质的相互转化和制备,",属于"常考题",熟悉题型是解题的关键。