服务热线
搜题▪组卷
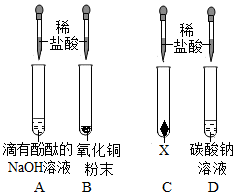 为验证“酸的化学通性”,某班同学在实验室进行了如下实验,请分析并回答相关问题
为验证“酸的化学通性”,某班同学在实验室进行了如下实验,请分析并回答相关问题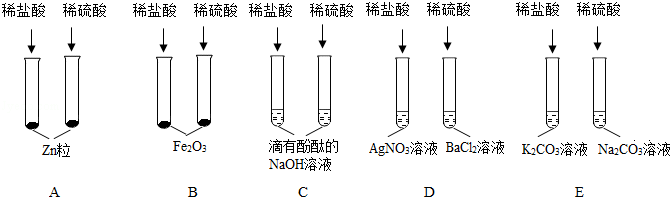
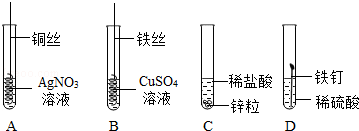
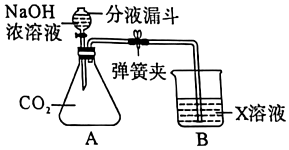
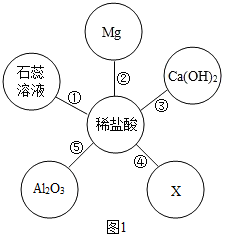
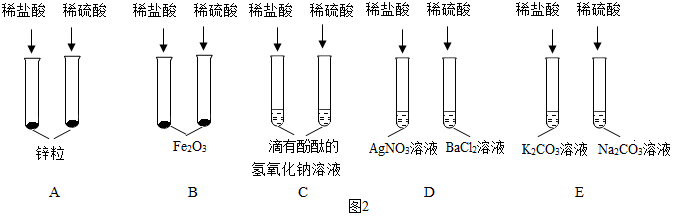
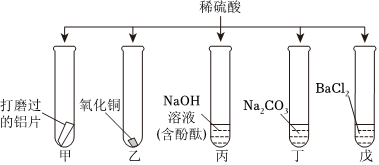
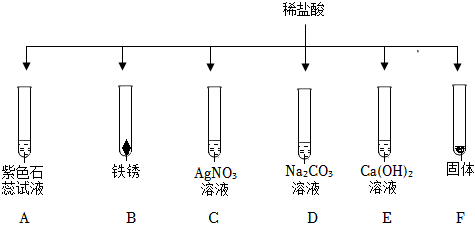
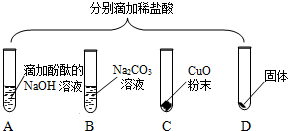 为验证“酸的化学通性”,某班同学在实验室进行如图实验。请分析并回答相关问题:
为验证“酸的化学通性”,某班同学在实验室进行如图实验。请分析并回答相关问题:
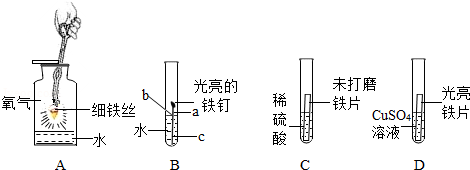
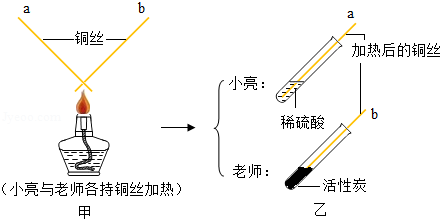

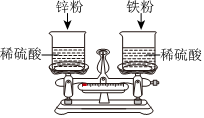 如图,托盘上各放一只等质量的烧杯,分别盛有等质量、等质量分数的稀硫酸,天平平衡,再向烧杯中分别加入等质量的铁粉和锌粉。
如图,托盘上各放一只等质量的烧杯,分别盛有等质量、等质量分数的稀硫酸,天平平衡,再向烧杯中分别加入等质量的铁粉和锌粉。
zki@dyw.com
2017-04-25
初中化学 | | 填空题