[考点]
金属的化学性质,一氧化碳还原氧化铁,书写化学方程式、文字表达式、电离方程式,
[解析]
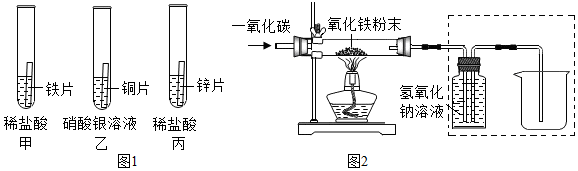
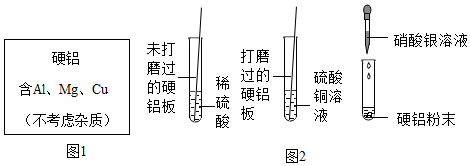
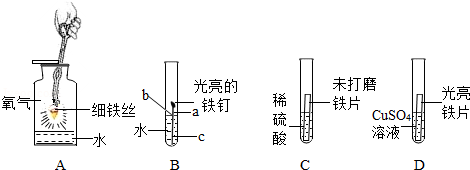
解:(1)A、甲试管中的实验现象为有气产生,溶液不是变为黄色,错误;
B、乙试管中铜和硝酸银反应生成银和硝酸铜,会导致反应后溶液的质量变小,错误;
C、实验室不用丙中原理制取H2,因为产生H2的中含有的HCl气体导致不纯,正确;
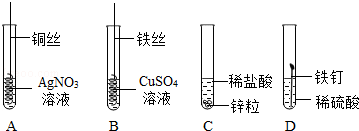
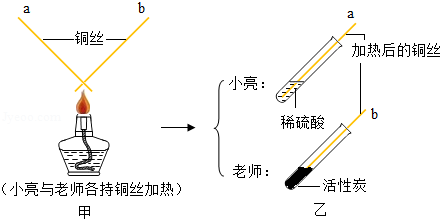
D、根据甲和丁,能证明锌和铁在氢前,且锌在铁的前面,通过乙能证明铜在银的前面,但是不知道铜是否在氢前还是氢后,为达到实验目的,还需要补充的实验是铜放入稀盐酸中而不是硫酸亚铁溶液中,错误;
故填:C;
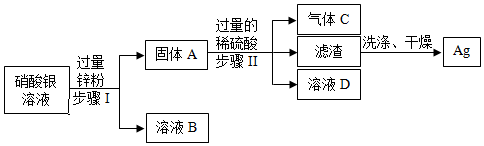
(2)乙试管中铜和硝酸银反应生成硝酸铜和银,故填:Cu+2AgNO3═Cu(NO3)2+2Ag;
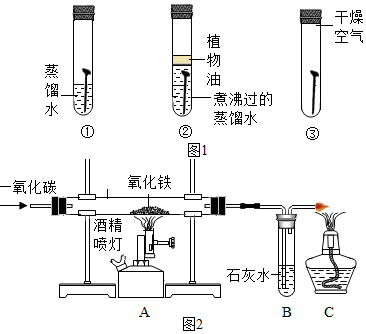
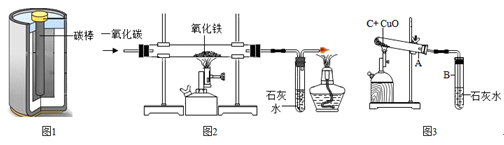
(3)A、实验过程中先通入一氧化碳后加热,目的是排出装置中空气,防止加热时爆炸,正确;
B、反应过程中硬质玻璃管内氧化铁被还原为铁,故现象为红棕色粉末变黑,正确;
C、装有氢氧化钠溶液的多功能瓶,其作用不仅为吸收二氧化碳,还能收集没有参加反应的一氧化碳,错误;
D.停止加热后,继续通入CO直至装置冷却,可防止氧气进入将铁再次氧化,正确;
故填:C。
[点评]
本题考查了"金属的化学性质,一氧化碳还原氧化铁,书写化学方程式、文字表达式、电离方程式,",属于"典型题",熟悉题型是解题的关键。
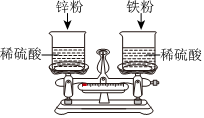 如图,托盘上各放一只等质量的烧杯,分别盛有等质量、等质量分数的稀硫酸,天平平衡,再向烧杯中分别加入等质量的铁粉和锌粉。
如图,托盘上各放一只等质量的烧杯,分别盛有等质量、等质量分数的稀硫酸,天平平衡,再向烧杯中分别加入等质量的铁粉和锌粉。
