[考点]
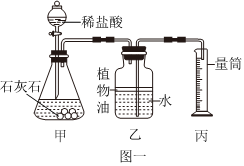
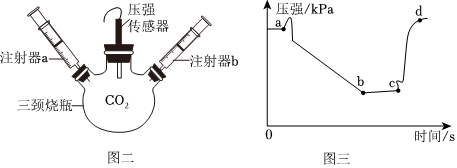
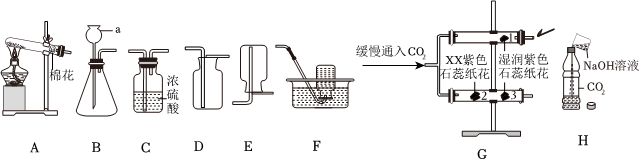
气体的净化(除杂),二氧化碳的实验室制法,制取二氧化碳实验的改进,
[答案]
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
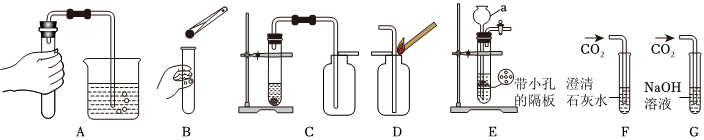
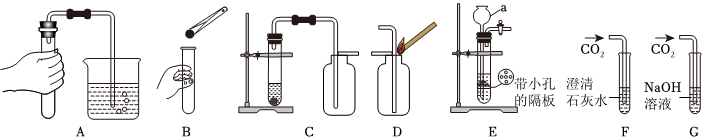
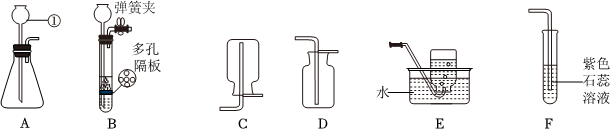
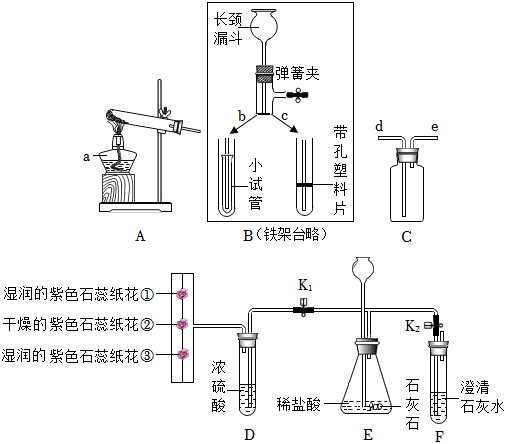
(2)D;C;E;
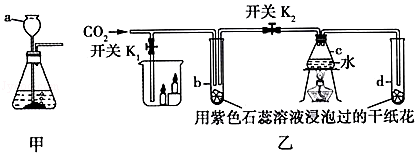
(3)能防止气体从长颈漏斗中逸出(或形成液封,控制反应的速率,合理即可)。
[解析]
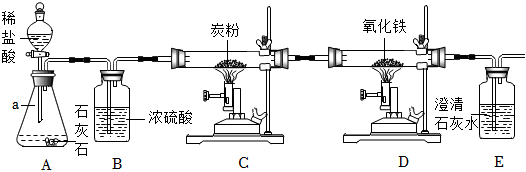
解:(1)实验室中常用石灰石与盐酸反应制取二氧化碳,石灰石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑。
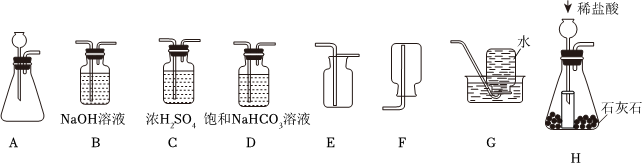
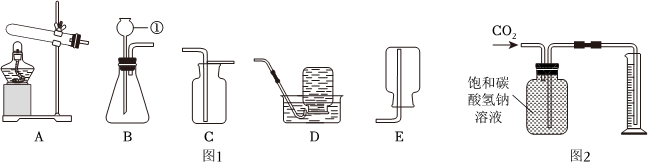
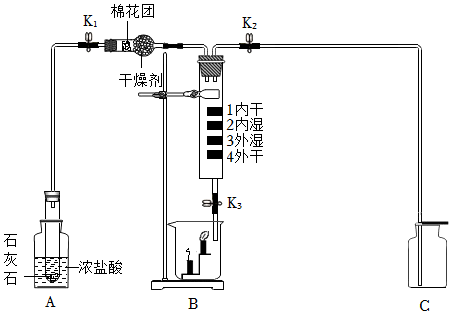
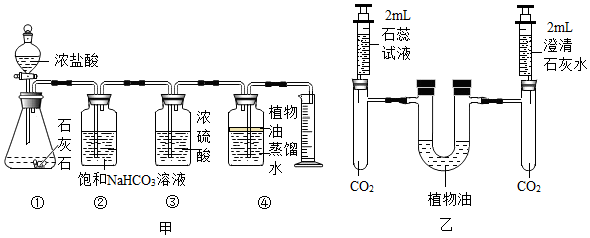
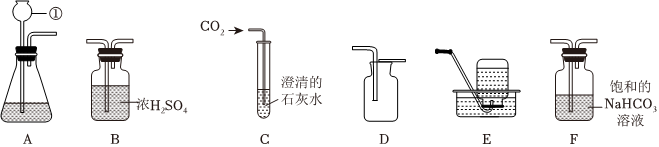
(2)制取的二氧化碳气体中混有氯化氢气体、水蒸气,除去氯化氢气体可用饱和碳酸氢钠溶液,除去水蒸气可用浓硫酸,要注意除水蒸气要放在最后去除,否则会再次引入水蒸气。为了得到干燥、纯净的CO2气体,产生的气流应依次通过装置D、C。
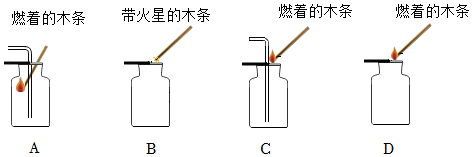
二氧化碳密度比空气大,能溶于水,应用向上排空气法收集,收集CO2气体选用的装置是E。
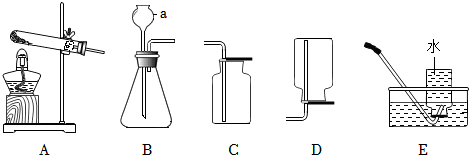
(3)在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中,如图H所示。改进后的优点是能防止气体从长颈漏斗中逸出或能形成液封,能通过加入稀盐酸的快慢,控制反应的速率(合理即可)。
故答案为:
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)D;C;E;
(3)能防止气体从长颈漏斗中逸出(或形成液封,控制反应的速率,合理即可)。
[点评]
本题考查了"气体的净化(除杂),二氧化碳的实验室制法,制取二氧化碳实验的改进,",属于"难典题",熟悉题型是解题的关键。