服务热线
搜题▪组卷
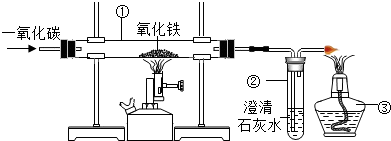
| 猜想 | 滤液成分 | 滤渣成分 |
| ① | AgNO3,Cu(NO3)2,Fe(NO3)2 | Ag |
| ② | Cu(NO3)2,Fe(NO3)2 | Ag、Fe |
| ③ | Cu(NO3)2,Fe(NO3)2 | Ag、Cu |
| ④ | Fe(NO3)2 | Ag、Cu |
| ⑤ | Fe(NO3)2 | Ag、Cu、Fe |
| 滤液 | 滤渣 | |
| 加入稀盐酸后现象 | 未出现白色沉淀 | 出现 |
| 结论 | 猜想 不成立 | 猜想⑤成立 |
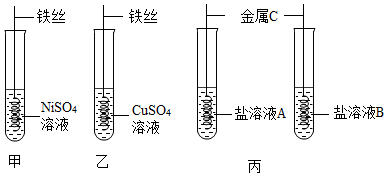
| 实验内容 | 实验步骤 | 实验现象 | 实验结论 |
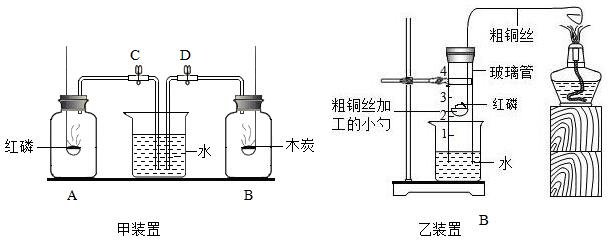
| 方法一 | 分别截取三片大小相同的金属片与试管中,加入等质量等浓度的稀盐酸。 | 甲表面产生气泡,乙表面无气泡,丙表面开始无气泡,一段时间后快速产生气泡。 | 甲>丙>乙 |
| 方法二 | 将上述试验中未反应完的金属片取出,用蒸馏水冲洗干净后,将乙、丙金属片分别放入盛有少量硫酸亚铁溶液的A、B试管中,充分反应。 | A试管中无明显现象; B试管中溶液由浅绿色变为无色 |
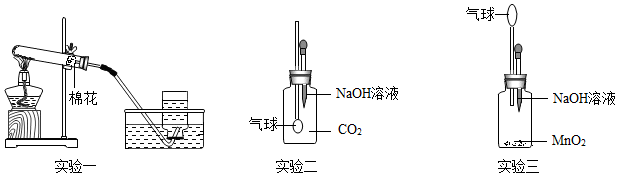
金属活动性由强到弱的顺序是 |
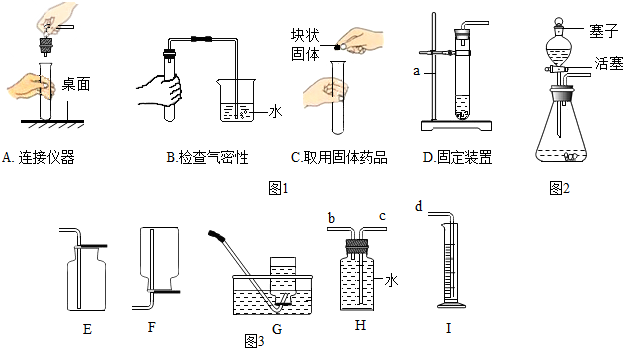
| 操作 | 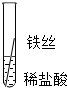 |
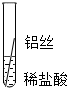 |
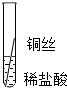 |
根据现象得出金属 活动性顺序 |
| 片刻后的现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
| 几分钟后的现象 | 有少量气泡 | 有大量气泡 | 无气泡 |
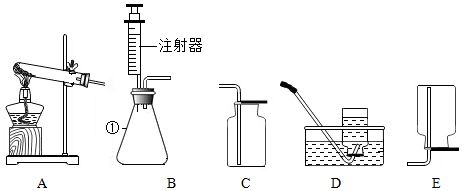
| 操作 | 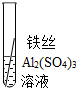 |
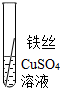 |
根据现象得出金属活动性顺序 |
| 现象 | Al>Fe>Cu |
| 甲同学 | 乙同学 | |
| 步骤 | 取少量废液于试管中,滴加AgNO3,溶液 | 取少量废液于试管中,滴加无色酚酞溶液 |
| 现象 | 产生白色沉淀 | 无变色现象 |
| 结论 | 废液中有HCl | 废液中无HCl |

lg@dyw.com
2016-02-27
初中化学 | 九年级上 | 实验题