[考点]
金属的物理性质及用途,合金与合金的性质,金属与氧气的反应,金属活动性强弱的判断,
[答案]
(1)延展;
(2)大;
(3)4Al+3O2═2Al2O3;
(4)D。
[解析]
解:(1)金属能加工成各种形状的器具,是利用了金属的延展性;
(2)合金的强度和硬度一般比组成它的纯金属更高,钢是铁的一种合金,其硬度比纯铁的硬度大;
(3)铝抗腐蚀性能好,是因为铝能与空气中的氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止内部的铝进一步氧化,反应的化学方程式为4Al+3O2=2Al2O3;
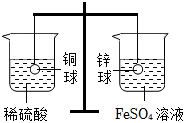
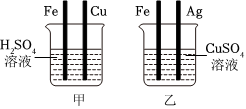
(4)A、在金属活动性顺序中,铜位于氢之后,不与稀硫酸反应,实验中观察到左端烧杯中无明显现象,故选项说法正确。
B、锌的金属活动性比铁强,和硫酸亚铁反应生成硫酸锌和铁,右端烧杯中反应后的溶液里一定有ZnSO4,故选项说法正确。
C、左端铜球质量不变,由Zn+FeSO4═ZnSO4+Fe可知,每65份质量的锌可置换出56份质量的铁,右端反应后锌球质量减小,因此取掉烧杯后,杠杆左端下沉,故选项说法正确。
D、左侧烧杯中无现象,说明铜的活动性比氢弱;右侧烧杯中锌能置换出硫酸亚铁溶液中的铁,说明锌的活动性比铁强,不能得出铁的金属活动性比铜强,故选项说法错误。
故答案为:(1)延展;
(2)大;
(3)4Al+3O2═2Al2O3;
(4)D。
[点评]
本题考查了"金属的物理性质及用途,合金与合金的性质,金属与氧气的反应,金属活动性强弱的判断,",属于"综合题",熟悉题型是解题的关键。
 三星堆是中华文明的瑰宝,出土了大量的青铜器文物。回答下列问题:
三星堆是中华文明的瑰宝,出土了大量的青铜器文物。回答下列问题: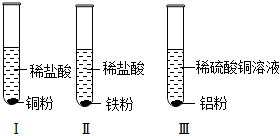
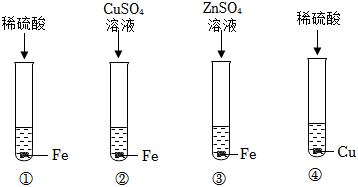
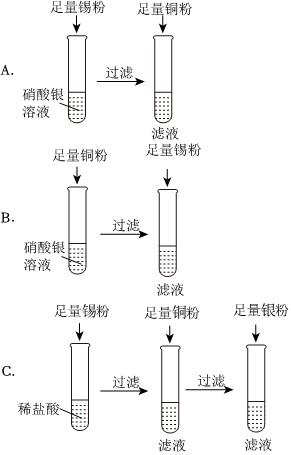
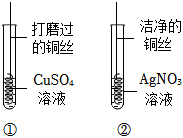 根据金属的性质回答下列问题。
根据金属的性质回答下列问题。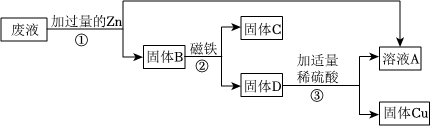
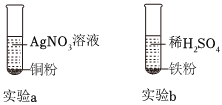
 实验中一个能发生反应的化学方程式 。
实验中一个能发生反应的化学方程式 。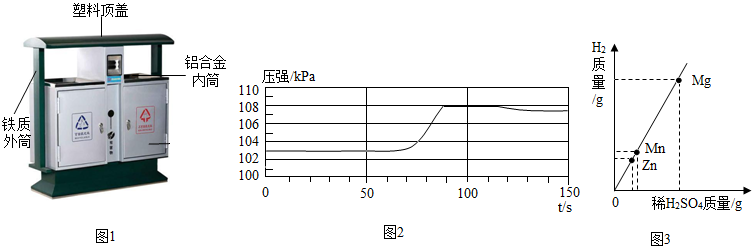 (1)空易拉罐应放入 (选填可回收物或其它垃圾)筒中。
(1)空易拉罐应放入 (选填可回收物或其它垃圾)筒中。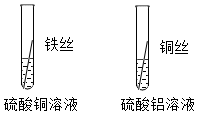 铁、铜、铝是生活中最常用的三种金属,小圆同学选取实验室提供的铁、铜、铝、稀硫酸、硫酸铜溶液、硫酸铝溶液,做了以下实验:
铁、铜、铝是生活中最常用的三种金属,小圆同学选取实验室提供的铁、铜、铝、稀硫酸、硫酸铜溶液、硫酸铝溶液,做了以下实验: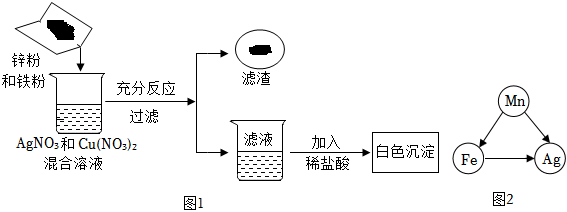
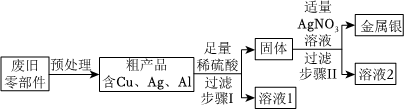
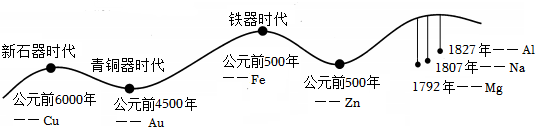
 人类文明进步与金属材料的发展关系密切。
人类文明进步与金属材料的发展关系密切。