服务热线
搜题▪组卷
 人类文明进步与金属材料的发展关系密切。
人类文明进步与金属材料的发展关系密切。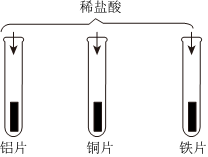 “神舟飞天”、“高铁奔驰”等中国制造,展现了中国智慧,增强了中华民族的自信心和自豪感,根据所学知识回答问题。
“神舟飞天”、“高铁奔驰”等中国制造,展现了中国智慧,增强了中华民族的自信心和自豪感,根据所学知识回答问题。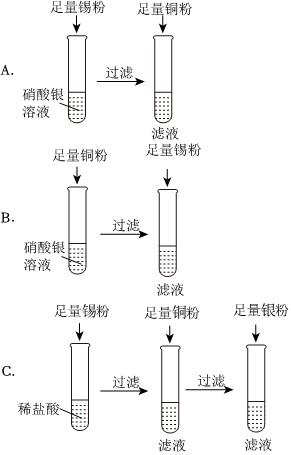
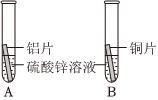 C919大飞机是我国自行研制、具有自主知识产权的大型喷气式民用飞机。
C919大飞机是我国自行研制、具有自主知识产权的大型喷气式民用飞机。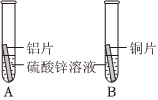 C919大飞机是我国自行研制、具有自主知识产权的大型喷气式民用飞机。
C919大飞机是我国自行研制、具有自主知识产权的大型喷气式民用飞机。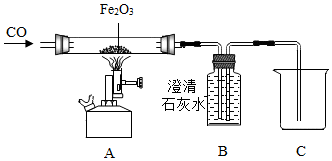 如图为实验室炼铁的改进装置,(部分夹持仪器略去),请回答下列问题。
如图为实验室炼铁的改进装置,(部分夹持仪器略去),请回答下列问题。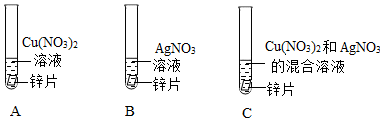
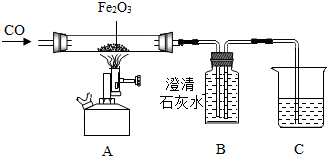 如图为实验室炼铁的改进装置,(部分夹持仪器略去),请回答下列问题。
如图为实验室炼铁的改进装置,(部分夹持仪器略去),请回答下列问题。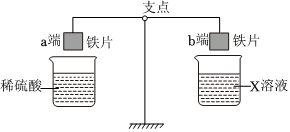 人类文明的发展和社会的进步与金属材料的关系十分密切。如图是有关金属的实验,实验前等臂杠杆两端悬挂等高度、等规格、等质量的铁片。请结合金属的相关知识分析以下问题。
人类文明的发展和社会的进步与金属材料的关系十分密切。如图是有关金属的实验,实验前等臂杠杆两端悬挂等高度、等规格、等质量的铁片。请结合金属的相关知识分析以下问题。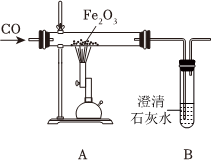 某化学兴趣小组同学利用图中一氧化碳与氧化铁反应所示装置模拟炼铁:
某化学兴趣小组同学利用图中一氧化碳与氧化铁反应所示装置模拟炼铁: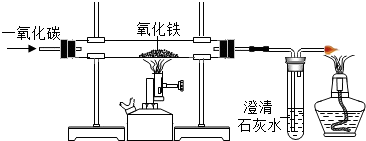
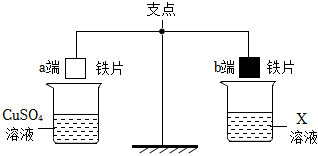 人类文明的发展和社会的进步与金属材料的关系十分密切。如图是有关金属的实验,请结合金属的相关知识分析以下问题。
人类文明的发展和社会的进步与金属材料的关系十分密切。如图是有关金属的实验,请结合金属的相关知识分析以下问题。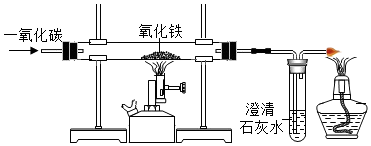 早在春秋战国时期,我们就开始生产和使用铁器.请按要求填空:
早在春秋战国时期,我们就开始生产和使用铁器.请按要求填空: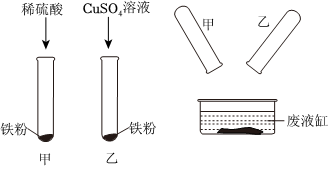

fik@dyw.com
2025-04-20
初中化学 | | 填空题