[考点]
金属的化学性质,盐的化学性质,常见离子的检验方法及现象,
[答案]
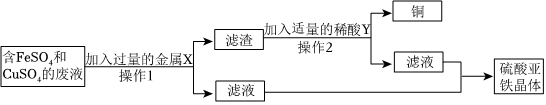
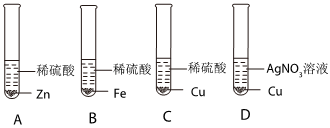
(1)Fe+CuSO4=FeSO4+Cu。
(2)Cu(OH)2;食醋;
(3)①Mg2+和Cl﹣;NO3﹣;
②防止实验a中加入了BaCl2溶液,影响Cl﹣的检验
[解析]
解:
(1)铁能与硫酸铜反应生成硫酸亚铁和铜,发生反应的化学方程式是:Fe+CuSO4=FeSO4+Cu。
(2)波尔多液中两种物质氢氧化钙与硫酸铜相互反应,生成蓝色的氢氧化铜沉淀,不溶于水,形成蓝色斑点,厨房用品中的食醋显酸性,可以和氢氧化铜反应置中和反应从而把氢氧化铜除去;
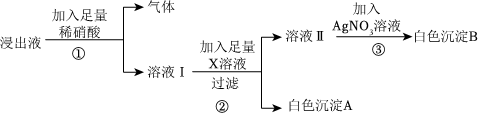
(3)a.取少量废液,向废液中滴加NaOH溶液,有白色沉淀生成,说明溶液中含有Mg2+,不含Fe3+;
另取少量废液,向其中滴加BaCl2溶液,无明显现象,说明溶液中不含SO42﹣ 和CO32﹣;
b.再取少量废液,滴加AgNO3溶液,产生白色沉淀,加稀硝酸后沉淀不溶解,说明溶液中含有Cl﹣。
①废液中一定含有的离子是Mg2+和Cl﹣,可能含有NO3﹣;
②实验b要验证是否含有Cl﹣,由于实验a中加入了BaCl2溶液,同样会与AgNO3溶液反应,产生白色沉淀,加稀硝酸后沉淀不溶解,影响Cl﹣的检验。
[点评]
本题考查了"金属的化学性质,盐的化学性质,常见离子的检验方法及现象",属于"综合题",熟悉知识点是解题的关键。


 ?
?

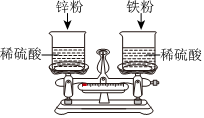 如图,托盘上各放一只等质量的烧杯,分别盛有等质量、等质量分数的稀硫酸,天平平衡,再向烧杯中分别加入等质量的铁粉和锌粉。
如图,托盘上各放一只等质量的烧杯,分别盛有等质量、等质量分数的稀硫酸,天平平衡,再向烧杯中分别加入等质量的铁粉和锌粉。