[考点]
化学实验方案设计与评价,常见气体的检验与除杂方法,氢气的化学性质与燃烧实验,
[解析]
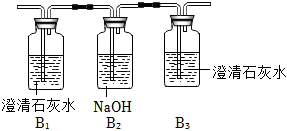
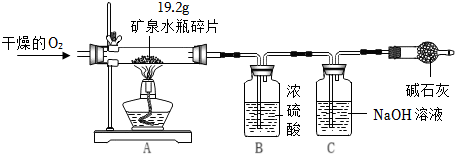
解:(1)在用锌粒与稀硫酸反应制取氢气时得到的氢气中往往含有水蒸气,需要除水蒸气,因B能吸收水分做干燥剂,所以装置C最后吸收水分的装置,故接口顺序为a→b→c→h→i→e→d→f→g,故填:h→i→e→d→f;
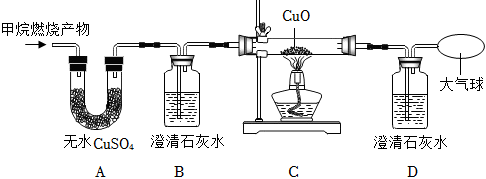
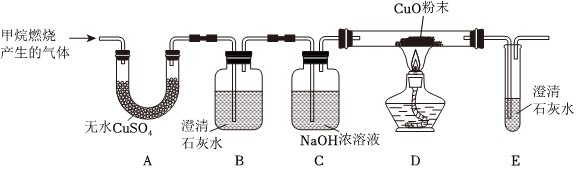
(2)任何可燃气体在加热时都不能混有空气,所以加热前应先把装置内的空气排净以防爆炸;故填:赶尽装置中的空气防止氢气与空气混合后受热爆炸;
(3)E装置减轻的质量就是CuO中的O失去的质量,是氢气夺走了CuO中的O生成了水,U形管增重的质量就是该反应生成的水的质量,则水中H元素的质量就是水的质量减去O元素的质量,则水的质量是147.2g﹣140.0g=7.2g;氧的质量是85.6g﹣79.2g=6.4g,所以氢气质量是7.2g﹣6.4g=0.8g;故填:7.2;0.8;
(4)D的作用是吸收空气中的水蒸气,以免进入C装置影响测定结果,若无D,空气中的水蒸气加入,洗气瓶的质量增加,E减少的质量不变,即所测氧的质量不变,则氢的质量增加,从而造成测量结果偏大。故填:偏大。
[点评]
本题考查了"化学实验方案设计与评价,常见气体的检验与除杂方法,氢气的化学性质与燃烧实验,",属于"典型题",熟悉题型是解题的关键。


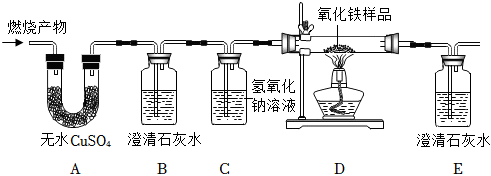
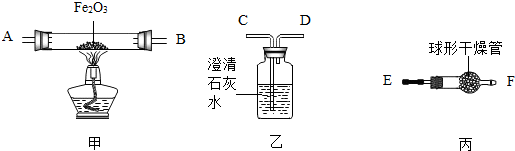
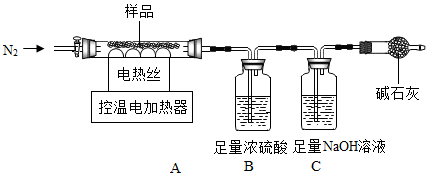
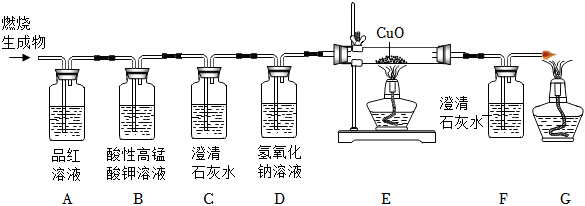
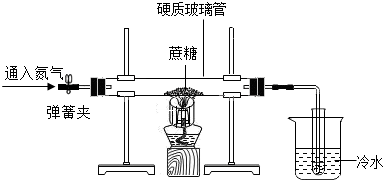
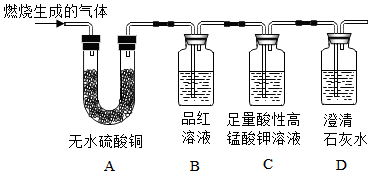 煤主要含有C、H、S三种元素,煤燃烧会对环境带来影响,化学兴趣小组对此进行实验探究(实验不考虑煤中含有的其他元素)。
煤主要含有C、H、S三种元素,煤燃烧会对环境带来影响,化学兴趣小组对此进行实验探究(实验不考虑煤中含有的其他元素)。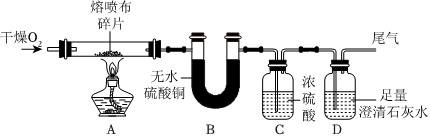
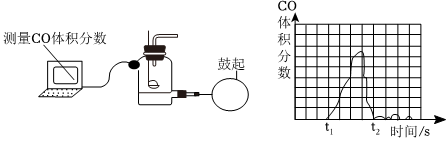
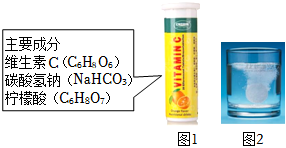 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。小组同学对产生的气体成分进行如下探究实验。
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。小组同学对产生的气体成分进行如下探究实验。