[考点]
金属的物理性质及用途,金属与氧气的反应,金属与盐溶液反应的原理,应用金属活动性解释相关现象,
[答案]
(1)延展;
(2)致密的氧化铝薄膜;
(3)ABC;
(4)ABCD。
[解析]
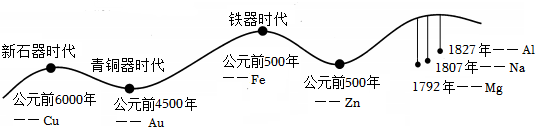
解(1)贴金技艺利用了金具有良好的延展性,将黄金锤打成极薄的薄片。
(2)铝的化学性质很活泼,铝制品缺不易锈蚀,原因是铝在常温下会与氧气反应形成一层致密的氧化铝薄膜,从而阻止铝进一步氧化。
(3)A、在相同的条件下,金属与氧气反应时,反应条件越简单,说明该金属的活动性越强,金属镁在空气中比铝更易点燃,说明镁比铝活动性强,故A正确;
B、用硫酸铜、石灰水配制农药波尔多液,不宜用铁制容器,是因为铁的活动性比铜强,能与硫酸铜发生置换反应,所以不能用铁制容器配制波尔多液,故B正确;
C、金属锌与稀硫酸反应速率适中,Mg、Al金属活动性比锌强,与稀硫酸反应速率较快,不便于气体收集,所以金属锌比Mg、Al等更适于实验室制取氢气,故C正确。
故选:ABC。
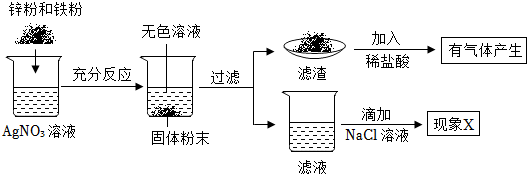
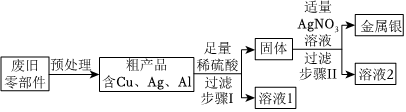
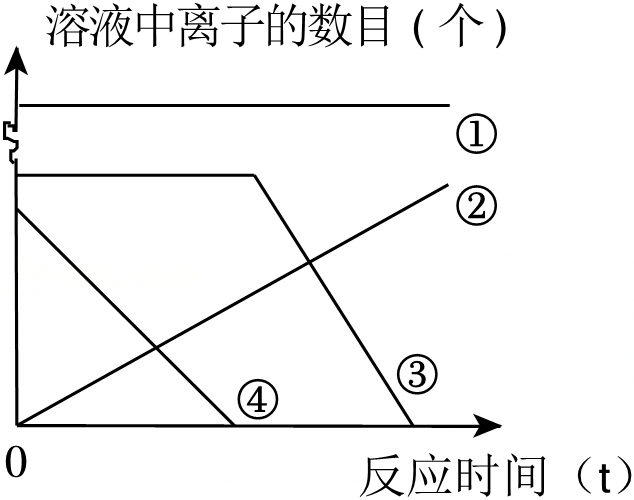
(4)三种金属的活动性:镁>铜>银,将镁粉投入一定量硝酸铜和硝酸银的混合溶液中,镁先与硝酸银反应,硝酸银反应完全以后,镁再与硝酸铜反应,反应的化学方程式分别为:Mg+2AgNO3=Mg(NO3)2+2Ag、Mg+Cu(NO3)2=Mg(NO3)2+Cu。
A、由反应方程式可知,溶液中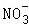 的数目不变,所以①表示溶液中
的数目不变,所以①表示溶液中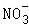 的数目随反应时间的变化情况,故选项正确;
B、由于镁先与硝酸银反应,银离子转化为银原子,溶液中Ag+数目逐渐减少,当硝酸银反应完全后,溶液中Ag+数目变为0,因此曲线为④,故选项正确;
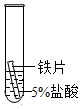
C、若滤液为无色,说明硝酸铜反应完全,如果镁粉过量,则向滤渣中加稀盐酸,会有气泡产生,如果镁粉恰好完全反应,则向滤渣中加稀盐酸,不会有气泡产生,故选项正确;
D、镁与硝酸银反应、镁与硝酸铜反应都有Mg2+生成,所以Mg2+数目逐渐增大,反应完毕以后不变,因此曲线为②,故选项正确。
故答案为:
(1)延展;
(2)致密的氧化铝薄膜;
(3)ABC;
(4)ABCD。
的数目随反应时间的变化情况,故选项正确;
B、由于镁先与硝酸银反应,银离子转化为银原子,溶液中Ag+数目逐渐减少,当硝酸银反应完全后,溶液中Ag+数目变为0,因此曲线为④,故选项正确;
C、若滤液为无色,说明硝酸铜反应完全,如果镁粉过量,则向滤渣中加稀盐酸,会有气泡产生,如果镁粉恰好完全反应,则向滤渣中加稀盐酸,不会有气泡产生,故选项正确;
D、镁与硝酸银反应、镁与硝酸铜反应都有Mg2+生成,所以Mg2+数目逐渐增大,反应完毕以后不变,因此曲线为②,故选项正确。
故答案为:
(1)延展;
(2)致密的氧化铝薄膜;
(3)ABC;
(4)ABCD。
[点评]
本题考查了"金属的物理性质及用途,金属与氧气的反应,金属与盐溶液反应的原理,应用金属活动性解释相关现象,",属于"综合题",熟悉题型是解题的关键。
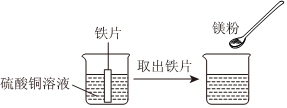
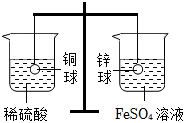
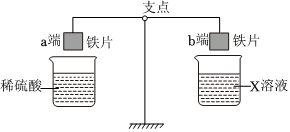 人类文明的发展和社会的进步与金属材料的关系十分密切。如图是有关金属的实验,实验前等臂杠杆两端悬挂等高度、等规格、等质量的铁片。请结合金属的相关知识分析以下问题。
人类文明的发展和社会的进步与金属材料的关系十分密切。如图是有关金属的实验,实验前等臂杠杆两端悬挂等高度、等规格、等质量的铁片。请结合金属的相关知识分析以下问题。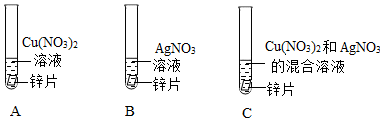
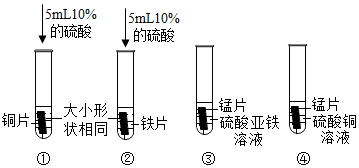
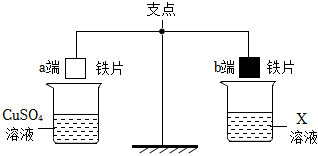 人类文明的发展和社会的进步与金属材料的关系十分密切。如图是有关金属的实验,请结合金属的相关知识分析以下问题。
人类文明的发展和社会的进步与金属材料的关系十分密切。如图是有关金属的实验,请结合金属的相关知识分析以下问题。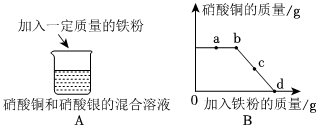
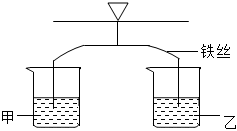 金属与我们的生活息息相关。
金属与我们的生活息息相关。