[考点]
金属的物理性质及用途,金属与盐溶液反应的原理,金属活动性强弱的判断,
[答案]
(1)延展;
(2)②;
(3)Fe+CuSO4=Cu+FeSO4;
(4)AB。
[解析]
解:(1)古代工匠把金块变成细细的金线来制作金缕衣,正是利用了金的延展性。
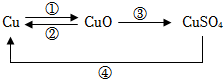
(2)在含铜物质的转化中,有一种黑色固体是氧化铜,而红色固体是金属铜。当氧化铜与某些物质(如氢气、碳等)发生反应时,黑色的氧化铜会变成红色的铜,这个过程会观察到固体由黑变红,对应反应①。
(3)“曾青得铁则化为铜”描述的是铁和硫酸铜溶液的反应。铁能把硫酸铜溶液里的铜置换出来,生成一种新的溶液(硫酸亚铁)和红色的铜单质,体现了铁的金属活动性比铜强,反应的化学方程式为Fe+CuSO4=Cu+FeSO4。
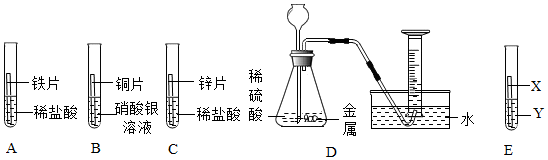
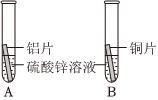
(4)A、铝片、铁片、硫酸铜溶液铝和铁都能与硫酸铜溶液反应,置换出红色的铜,说明铝和铁都比铜活泼,但无法知道铝和铁谁更活泼(缺少铝和铁直接比较的证据),试剂选择错误。
B、铜片、硫酸铝溶液、硫酸亚铁溶液铜片与硫酸铝溶液、硫酸亚铁溶液都不反应,说明铜最不活泼,但缺少铝和铁直接比较的实验,故错误。
C、铜片、铝片、铁片、稀硫酸铝和铁都能与稀硫酸反应产生气泡,但铝反应更剧烈,说明铝比铁活泼;铜不与稀硫酸反应,说明铜最不活泼,可得出铝>铁>铜,故正确。
D、铁片、硫酸铝溶液、硫酸铜溶液铁片与硫酸铝溶液不反应,说明铁不如铝活泼;铁片与硫酸铜溶液反应,置换出铜,说明铁比铜活泼,可得出铝>铁>铜,故正确。
故答案为:
(1)延展;
(2)②;
(3)Fe+CuSO4=Cu+FeSO4;
(4)AB。
[点评]
本题考查了"金属的物理性质及用途,金属与盐溶液反应的原理,金属活动性强弱的判断,",属于"难典题",熟悉题型是解题的关键。
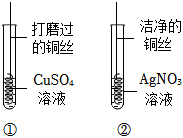 根据金属的性质回答下列问题。
根据金属的性质回答下列问题。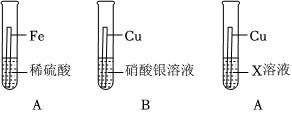
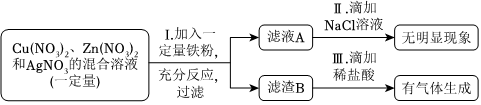
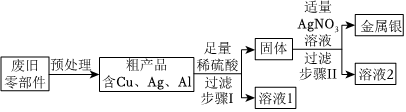
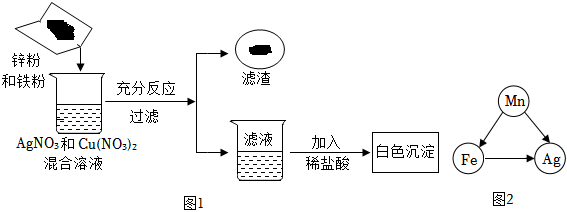
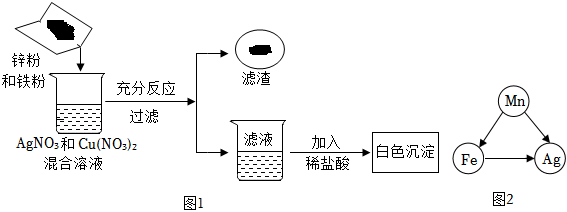
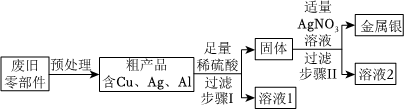
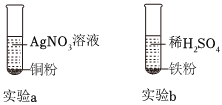 三星堆是中华文明的瑰宝,出土了大量的青铜器文物。回答下列问题:
三星堆是中华文明的瑰宝,出土了大量的青铜器文物。回答下列问题: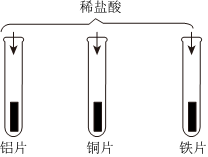 “神舟飞天”、“高铁奔驰”等中国制造,展现了中国智慧,增强了中华民族的自信心和自豪感,根据所学知识回答问题。
“神舟飞天”、“高铁奔驰”等中国制造,展现了中国智慧,增强了中华民族的自信心和自豪感,根据所学知识回答问题。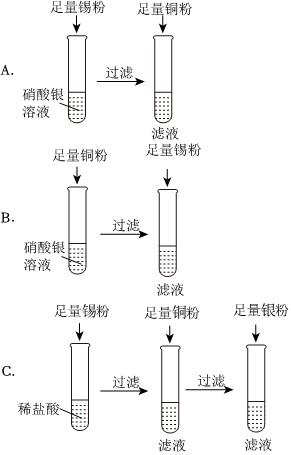
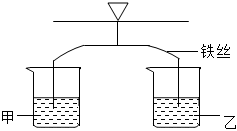 金属与我们的生活息息相关。
金属与我们的生活息息相关。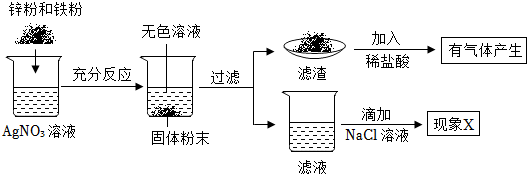
 C919大飞机是我国自行研制、具有自主知识产权的大型喷气式民用飞机。
C919大飞机是我国自行研制、具有自主知识产权的大型喷气式民用飞机。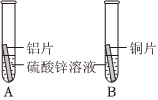 C919大飞机是我国自行研制、具有自主知识产权的大型喷气式民用飞机。
C919大飞机是我国自行研制、具有自主知识产权的大型喷气式民用飞机。