[考点]
药品是否变质的探究,碱的化学性质,盐的化学性质,
[答案]
(1)2NaOH+CO2=Na2CO3+H2O;
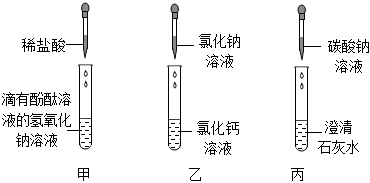
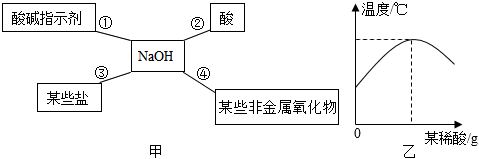
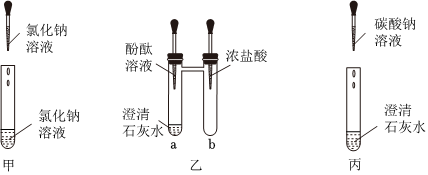
(2)碳酸钠溶液和氢氧化钠溶液都显碱性,都能使无色酚酞溶液变红;
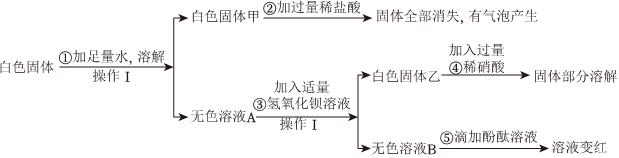
(3)有白色沉淀生成且溶液为红色;
(4)CaCl2、NaOH。
[解析]
解:(1)NaOH溶液变质是氢氧化钠与空气中的二氧化碳反应生成了碳酸钠和水,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O;
(2)溶液a呈红色,不能说明NaOH溶液变质,是因为碳酸钠溶液和氢氧化钠溶液都显碱性,都能使无色酚酞溶液变红;
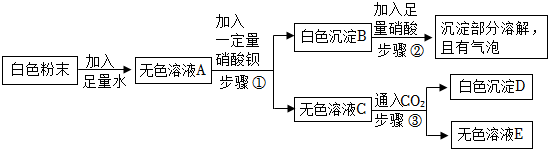
(3)“现象”是有白色沉淀生成且溶液为红色,说明NaOH溶液部分变质,溶质中含有氢氧化钠和碳酸钠,碳酸钠与过量氯化钙反应生成碳酸钙沉淀,氢氧化钠使无色酚酞溶液变红;
(4)X溶液中含有的2种溶质是CaCl2、NaOH,由强酸制弱酸可知,二氧化碳通入氯化钙溶液不发生反应,而二氧化碳通入氯化钙和氢氧化钠的混合溶液可以看到有白色沉淀生成,说明二氧化碳能与氢氧化钠溶液反应生成碳酸钠,碳酸钠进一步与氯化钙反应生成碳酸钙沉淀。
故答案为:(1)2NaOH+CO2=Na2CO3+H2O;
(2)碳酸钠溶液和氢氧化钠溶液都显碱性,都能使无色酚酞溶液变红;
(3)有白色沉淀生成且溶液为红色;
(4)CaCl2、NaOH。
[点评]
本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。

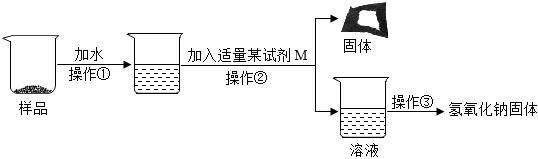
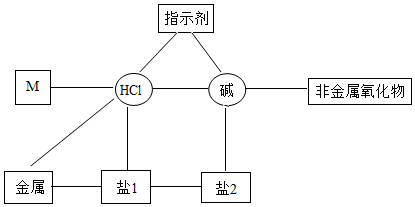
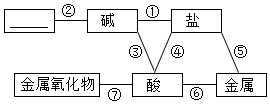 归纳是学习化学的重要方法。小明总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应)。若图中的酸为盐酸,根据题目回答下面的问题。
归纳是学习化学的重要方法。小明总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应)。若图中的酸为盐酸,根据题目回答下面的问题。