服务热线
搜题▪组卷
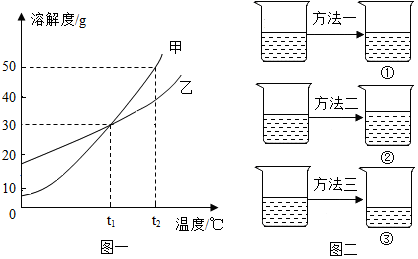
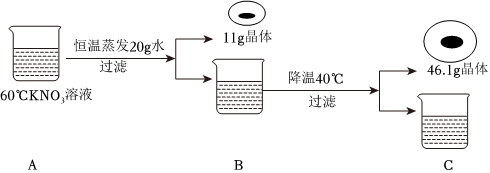
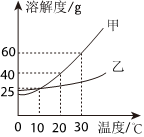 如图是甲、乙两种固体物质的溶解度曲线。据图回答:
如图是甲、乙两种固体物质的溶解度曲线。据图回答: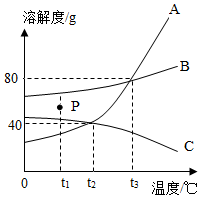
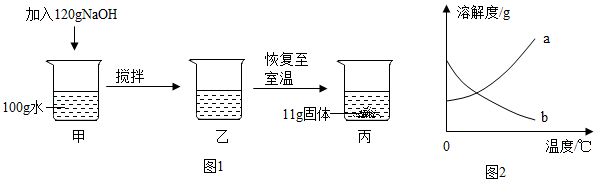
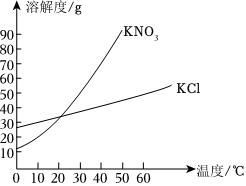
 如图是甲、乙、丙三种固体物质(受热均不分解,且晶体均不含结晶水)在水中的溶解度曲线。请据图回答下列问题:
如图是甲、乙、丙三种固体物质(受热均不分解,且晶体均不含结晶水)在水中的溶解度曲线。请据图回答下列问题:
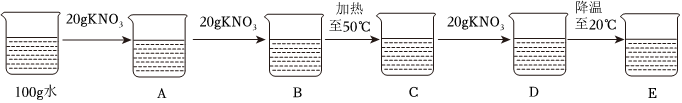
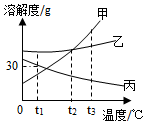
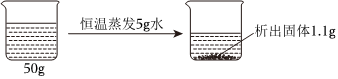
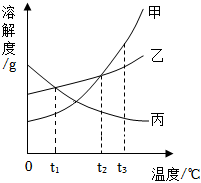 如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答下列问题。
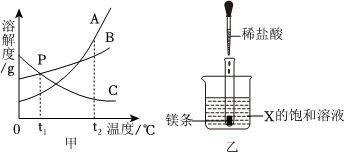
如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答下列问题。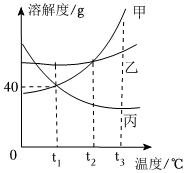 甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答下列问题。
甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答下列问题。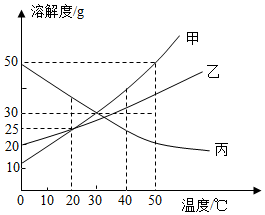

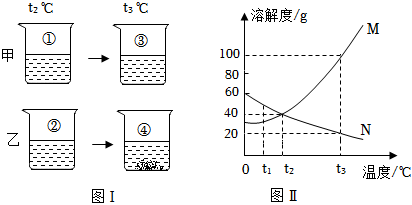
| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | |
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | M | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 |
| N | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |

| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| (g/100g水) | NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |

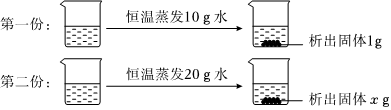
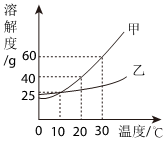 如图是甲、乙两种固体物质的溶解度曲线。据图回答:?
如图是甲、乙两种固体物质的溶解度曲线。据图回答:?
bjj@dyw.com
2016-06-09
初中化学 | | 填空题