[考点]
实验探究物质的组成成分以及含量,酸的化学性质,碱的化学性质,盐的化学性质,
[解析]
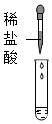
解:(1)产生气泡,是因为左边试管中的硫酸过量,右边试管中的碳酸钠过量,碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳,反应的反应方程式为:H2SO4+Na2CO3═Na2SO4+H2O+CO2↑。
故填:H2SO4+Na2CO3═Na2SO4+H2O+CO2↑。
(2)【作出猜想】
猜想一:碳酸钠和稀硫酸恰好完全反应时溶质为Na2SO4
猜想二:稀硫酸过量时溶质为Na2SO4和H2SO4;
猜想三:碳酸钠过量时溶质为Na2SO4和Na2CO3;
故填:Na2SO4和H2SO4。
【表达交流】
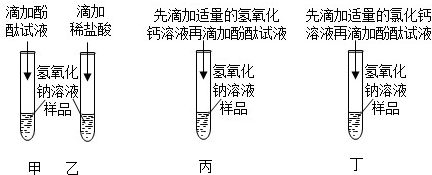
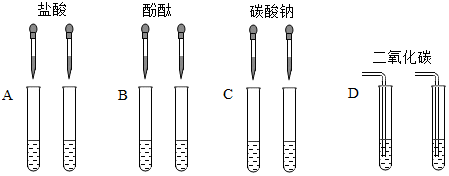
①实验一溶液变红的原因是碳酸钠溶液呈碱性。
故填:碳酸钠溶液呈碱性。
②小羽认为实验二的方案是错误的,原因是含有硫酸钠或硫酸钠和硫酸时,加入氯化钡也能够产生白色沉淀。
故填:含有硫酸钠或硫酸钠和硫酸时,加入氯化钡也能够产生白色沉淀。
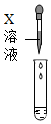
③实验四用到的X溶液的物质类别与上述三种试剂不同,则X溶液溶质的化学式是Ca(OH)2,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,过程中产生白色沉淀。
故填:Ca(OH)2。
【反思与评价】
将上述废液加水稀释后可与油污反应,从而去除油污,发生了化学变化;
厨房常用洗洁精清洗餐具上的油污,是因为洗洁精能够乳化油污;
用汽油除去衣服上的油污,是因为汽油能够溶解油污。
故填:A。
[点评]
本题考查了"实验探究物质的组成成分以及含量,酸的化学性质,碱的化学性质,盐的化学性质,",属于"综合题",熟悉题型是解题的关键。
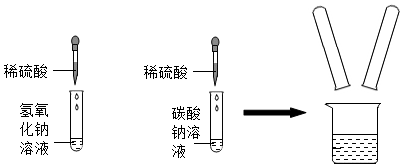
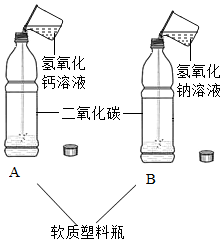 实验室在做有关CO2的性质实验中,用氢氧化钠溶液吸收CO2,而不用澄清石灰水,小喵同学想用以下A、B两组对比试验进行验证(实验后立即盖紧瓶盖并振荡);
实验室在做有关CO2的性质实验中,用氢氧化钠溶液吸收CO2,而不用澄清石灰水,小喵同学想用以下A、B两组对比试验进行验证(实验后立即盖紧瓶盖并振荡);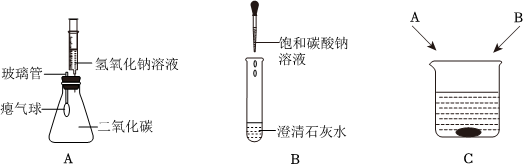

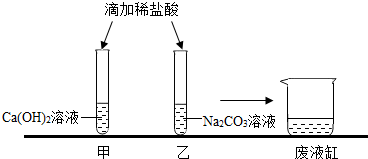 实验结束,甲、乙同学依次将废液缓慢倒入同一洁净的废液缸中,然后进行了讨论。
实验结束,甲、乙同学依次将废液缓慢倒入同一洁净的废液缸中,然后进行了讨论。