[考点]
实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式,
[解析]
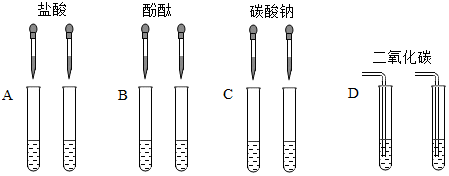
解:①乙同学认为,甲同学实验时向氢氧化钙溶液中应先滴几滴酚酞试液,再滴加适量的稀盐酸,当观察到红色逐渐变浅直至无色时,就可以说明两种物质能发生反应。
故填:红色逐渐变浅直至无色。
②稀盐酸和氢氧化钙反应生成氯化钙和水,反应的化学方程式为:Ca( OH)2+2HCl=CaCl2+2H2O。
故填:Ca( OH)2+2HCl=CaCl2+2H2O。
③当乙同学沿废液缸内壁缓慢倾倒液体时,观察到废液缸中先有气泡产生,然后又出现了白色沉淀,说明甲中稀盐酸过量,即甲中溶质是氯化钙和氯化氢。
故填:CaCl2、HCl。
④当乙同学沿废液缸内壁缓慢倾倒液体时,观察到废液缸中先有气泡产生,然后又出现了白色沉淀,说明乙中碳酸钠过量,即乙中溶质是氯化钠和碳酸钠。
故填:NaCl、Na2CO3。
⑤取少量废液于试管中,向其中滴加氯化钙溶液,出现白色沉淀,说明溶液中含有碳酸钠。
故填:氯化钙。
⑥乙同学认为甲同学的结论不正确,理由是甲只能说明废液中没CaCl2,如果溶液中只有NaCl时,试管中也无明显现象。
故填:甲只能说明废液中没CaCl2,如果溶液中只有NaCl时,试管中也无明显现象。
⑦甲、乙同学确认了最终废液中溶质的成分是氯化钠和碳酸钠,处理该废液的方法是向最终溶液中加入适量氯化钙溶液(或稀盐酸),至中性后再倒掉。
故填:向最终溶液中加入适量氯化钙溶液(或稀盐酸),至中性后再倒掉。
[点评]
本题考查了"实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式,",属于"综合题",熟悉题型是解题的关键。
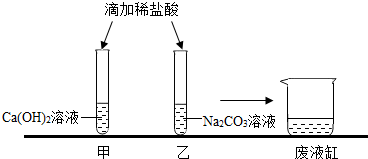 实验结束,甲、乙同学依次将废液缓慢倒入同一洁净的废液缸中,然后进行了讨论。
实验结束,甲、乙同学依次将废液缓慢倒入同一洁净的废液缸中,然后进行了讨论。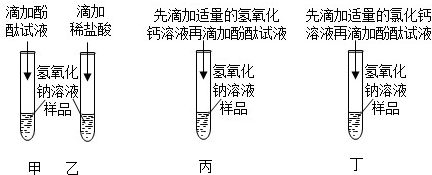
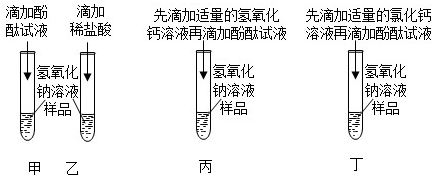
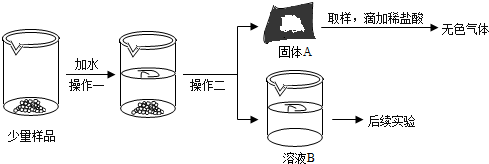
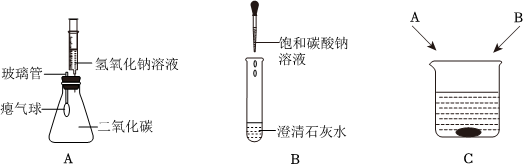
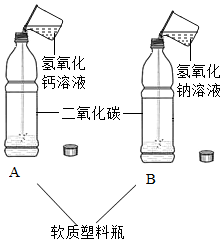 实验室在做有关CO2的性质实验中,用氢氧化钠溶液吸收CO2,而不用澄清石灰水,小喵同学想用以下A、B两组对比试验进行验证(实验后立即盖紧瓶盖并振荡);
实验室在做有关CO2的性质实验中,用氢氧化钠溶液吸收CO2,而不用澄清石灰水,小喵同学想用以下A、B两组对比试验进行验证(实验后立即盖紧瓶盖并振荡);