[答案]
(1)大;
(2)①ZnSO4、Al2(SO4)3、H2SO4;Cu+2AgNO3═Cu(NO3)2+2Ag;②Fe(合理即可)。
[解析]
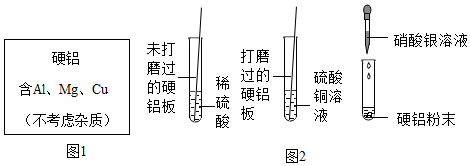
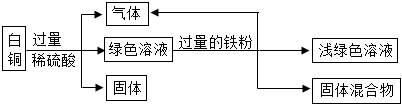
解:(1)合金的硬度大于其组成中纯金属的硬度,钢是铁与的合金,则硬度大于纯铁。
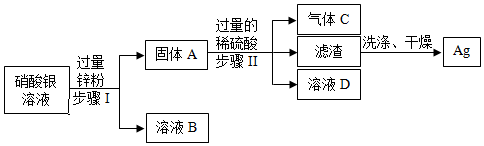
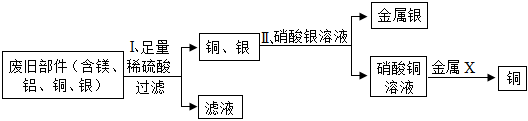
(2)①步骤Ⅰ为向含Zn、Al、Cu、Ag的部件中加入足量的稀硫酸,金属活动性是Al>Zn>H>Cu>Ag,则Zn能与H2SO4反应生成ZnSO4与H2,Al能与H2SO4反应生成Al2(SO4)3与H2,反应后溶液中溶质为:ZnSO4、Al2(SO4)3、H2SO4。
金属活动性Cu>Ag,则Cu能与硝酸银反应生成硝酸铜与银,反应的化学方程式为:Cu+2AgNO3═Cu(NO3)2+2Ag。
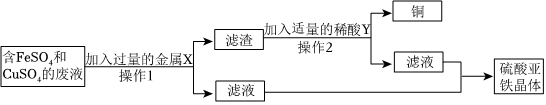
②金属活动性Fe>Cu,则Fe能与硝酸铜反应生成硝酸亚铁与铜,故金属X可以为Fe(合理即可)。
故答案为:
(1)大;
(2)①ZnSO4、Al2(SO4)3、H2SO4;Cu+2AgNO3═Cu(NO3)2+2Ag;②Fe(合理即可)。
[点评]
本题考查了"合金与合金的性质,金属的化学性质,",属于"必考题",熟悉题型是解题的关键。
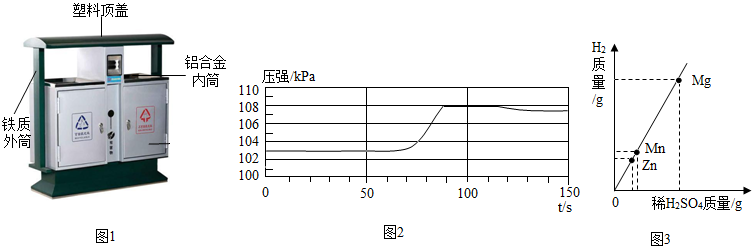 (1)空易拉罐应放入 (选填可回收物或其它垃圾)筒中。
(1)空易拉罐应放入 (选填可回收物或其它垃圾)筒中。