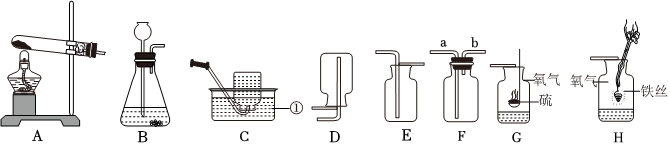
[考点]
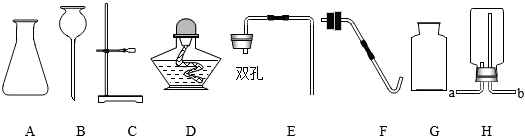
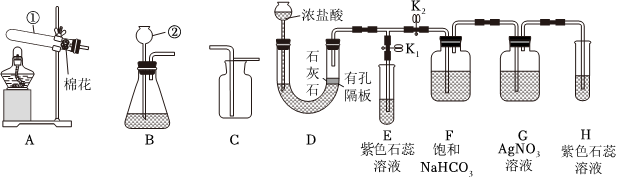
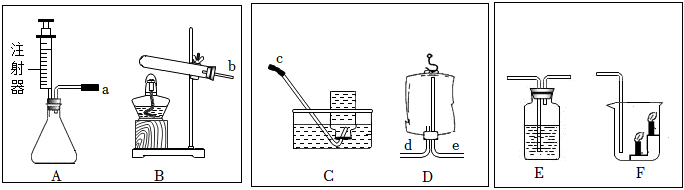
气体的干燥(除水),二氧化碳的实验室制法,二氧化碳的化学性质,一氧化碳还原氧化铁,
[答案]
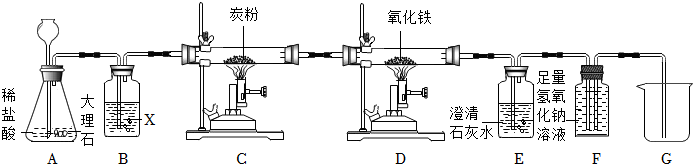
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)浓硫酸;
(3)红棕色固体逐渐变黑;
(4)不能;
(5)吸收二氧化碳并收集一氧化碳。
[解析]
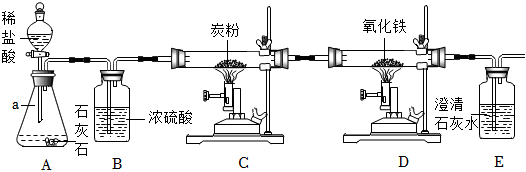
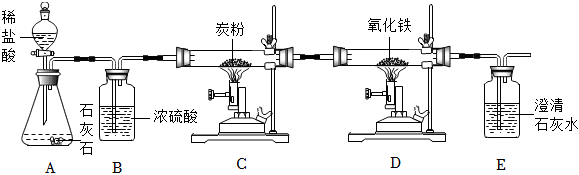
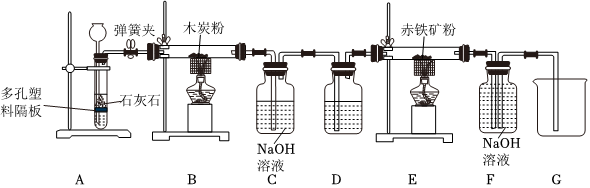
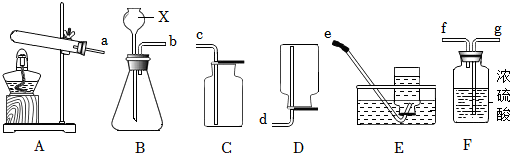
解:(1)大理石与稀盐酸反应生成氯化钙、二氧化碳和水,A中反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)由于C中要发生炭粉与二氧化碳高温下的反应,因此需要除去水蒸气,避免试管炸裂,因此B中盛放浓硫酸,做气体的干燥剂;
(3)C中产生一氧化碳进入D装置中,与氧化铁高温下反应生成铁和二氧化碳,因此D中可观察到的现象是红棕色固体逐渐变黑;
(4)E中澄清石灰水变浑浊,则有二氧化碳气体存在,但由于A中也会产生二氧化碳,而C、D之间没有接一个吸收二氧化碳气体的装置,无法确定二氧化碳是A中产生的,还是D中产生的,所以不能证明D中有二氧化碳气体产生;
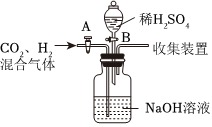
(5)一氧化碳与氢氧化钠溶液不反应,二氧化碳能够与氢氧化钠溶液反应;装置F中盛放的是氢氧化钠溶液,既能吸收二氧化碳气体的作用是吸收二氧化碳并收集一氧化碳;
故答案为:
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)浓硫酸;
(3)红棕色固体逐渐变黑;
(4)不能;
(5)吸收二氧化碳并收集一氧化碳。
[点评]
本题考查了"气体的干燥(除水),二氧化碳的实验室制法,二氧化碳的化学性质,一氧化碳还原氧化铁,",属于"综合题",熟悉题型是解题的关键。