[考点]
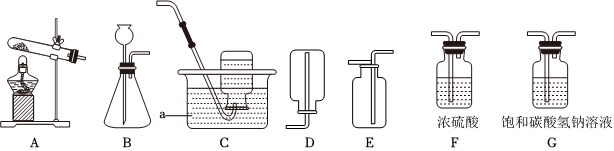
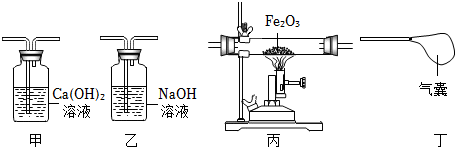
常用气体的发生装置和收集装置与选取方法,气体的干燥(除水),二氧化碳的物理性质,二氧化碳的化学性质,
[答案]
(1)分液;
(2)bd;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;浓硫酸;
(4)密度比空气大。
[解析]
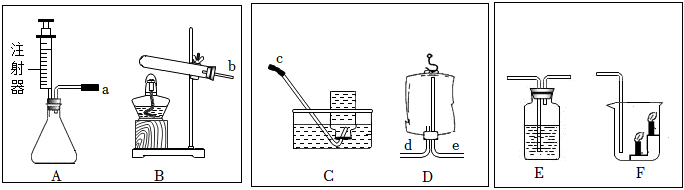
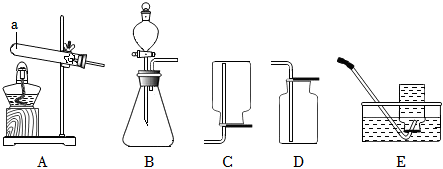
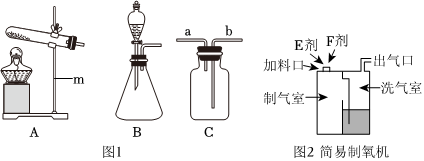
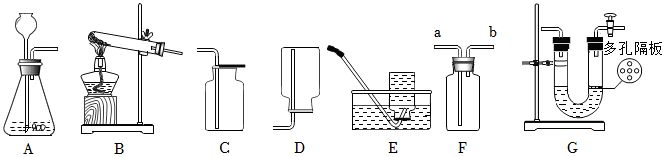
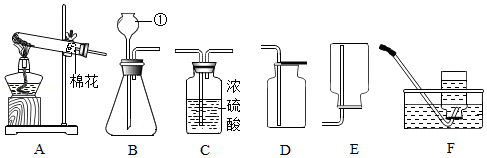
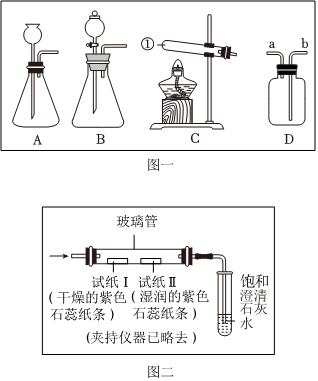
解:(1)利用装置A制取气体,便于控制反应速率,该注射器为实验代用品,注射器能通过控制液体的滴加速率来控制反应速率,其作用等同于分液漏斗。
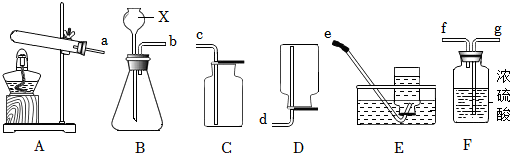
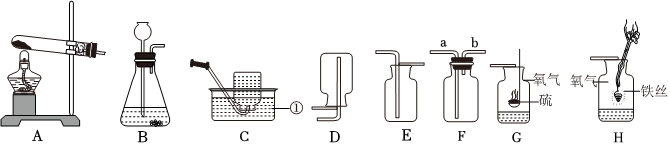
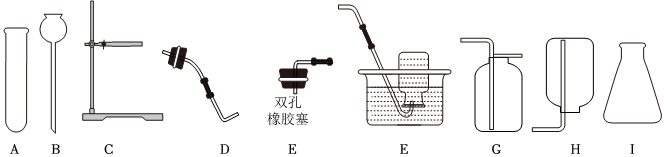
(2)若选用BD装置制取氧气时,氧气的密度比空气大,要通入D装置的下部,将空气向上排出,则导管口连接顺序为:bd。
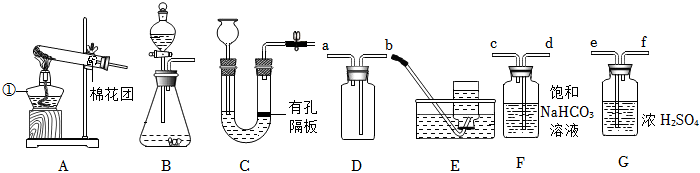
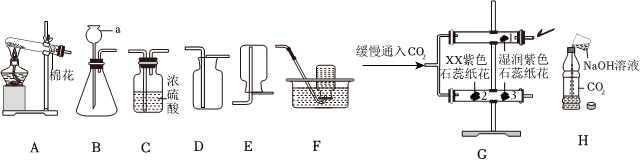
(3)实验室制备二氧化碳的反应是碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;浓硫酸具有吸水性,能干燥二氧化碳,若使用E装置干燥二氧化碳,可向瓶中加入适量的浓硫酸。
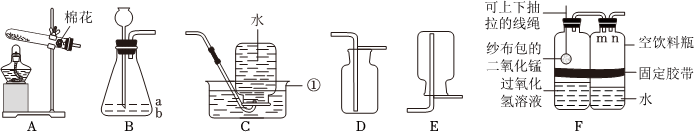
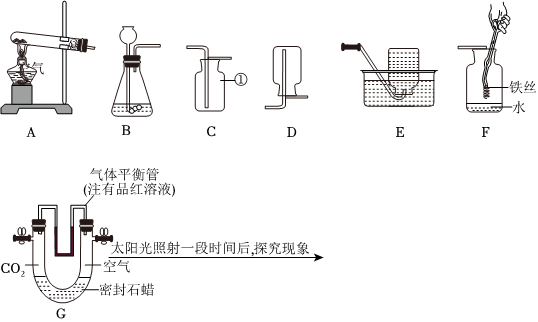
(4)F装置中,下方的蜡烛先熄灭,上方的蜡烛后熄灭,则根据F装置的相应现象,可得出二氧化碳的物理性质是:密度比空气大。
故答案为:
(1)分液;
(2)bd;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;浓硫酸;
(4)密度比空气大。
[点评]
本题考查了"常用气体的发生装置和收集装置与选取方法,气体的干燥(除水),二氧化碳的物理性质,二氧化碳的化学性质,",属于"综合题",熟悉题型是解题的关键。