[考点]
金属的化学性质,金属活动性顺序及其应用,金属锈蚀的条件及其防护,书写化学方程式、文字表达式、电离方程式,
[答案]
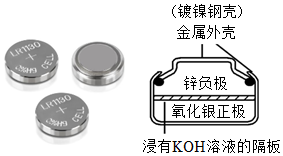
(1)隔绝氧气和水;
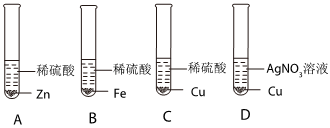
(2)Ag;
(3)Fe+H2SO4=FeSO4+H2↑或Zn+H2SO4=ZnSO4+H2↑;
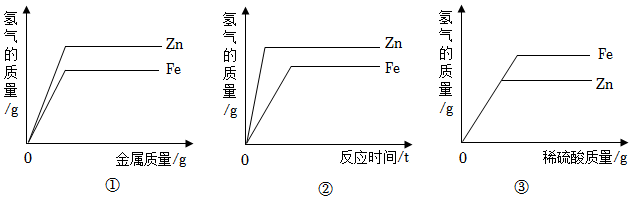
(4)③。
[解析]
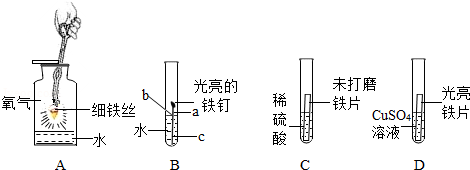
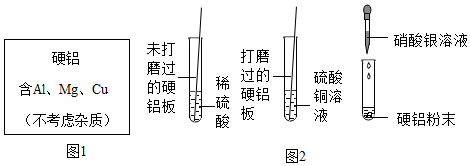
解:(1)金属防锈需要隔绝氧气和水,题干中镀镍,镍不容易与氧气反应,且可以隔绝内层金属与氧气、水接触,从而达到防锈目的,故答案为:隔绝氧气和水。
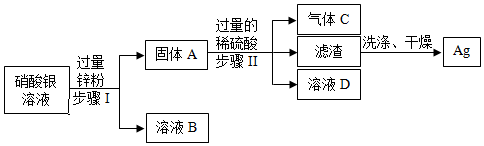
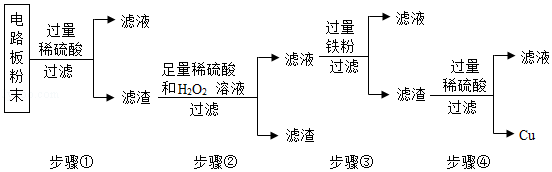
(2)金属置换的原理,金属活动性顺序强的,能把金属活性弱的置换出来,金属活动性Zn>Fe>Ag,故该金属的盐溶液所含的金属是银,元素符号为Ag,故答案为:Ag。
(3)铁、锌都能与稀硫酸反应,铁和稀硫酸反应生成硫酸亚铁和氢气,反应方程式为Fe+H2SO4=FeSO4+H2↑;锌和稀硫酸反应生成硫酸锌和氢气,其化学方程式为:Zn+H2SO4=ZnSO4+H2↑,故答案为:Fe+H2SO4=FeSO4+H2↑或Zn+H2SO4=ZnSO4+H2↑。
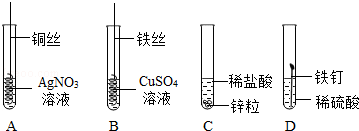
(4)等质量的金属和足量酸反应,化合价相同时,相对原子质量越小的产生氢气越多,铁和锌化合价相同,相对原子质量Fe<Zn,故Fe产生氢气多,故①②项错误;等质量的锌和铁与稀硫酸反应,刚开始酸不足,由于产生的氢气全部来自稀硫酸中氢元素,则生成的氢气的质量相同,最终金属反应完,56份质量的铁生成2份质量的氢气,65份质量的锌生成2份质量的氢气,向等质量、等质量分数的稀硫酸中,分别加入足量的铁粉和锌粉,铁产生氢气质量较大,③正确。
故选③。
[点评]
本题考查了"金属的化学性质,金属活动性顺序及其应用,金属锈蚀的条件及其防护,书写化学方程式、文字表达式、电离方程式,",属于"综合题",熟悉题型是解题的关键。